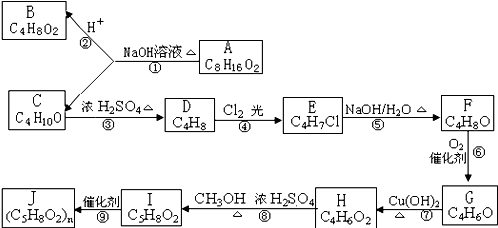
AЎўBЎўCЎўDЛДЦЦ¶МЦЬЖЪФӘЛШЈ¬AЎўBЎўCН¬ЦЬЖЪЈ¬AөДФӯЧУ°лҫ¶КЗН¬ЦЬЖЪЦРЧоҙуөДЈ»BЎўDН¬ЦчЧеЈ®јәЦӘDФӘЛШөДТ»ЦЦөҘЦККЗИХіЈЙъ»оЦРТыЛ®»ъіЈУГөДПы¶ҫјБЈ¬CФӘЛШөДөҘЦКҝЙТФҙУAЎўBБҪФӘЛШЧйіЙөД»ҜәПОпөДЛ®ИЬТәЦРЦГ»»іцBФӘЛШөДөҘЦКЈ®
ЈЁ1Ј©CФӘЛШФЪЦЬЖЪұнЦРөДО»ЦГ
өЪИэЦЬЖЪЈ¬өЪVIIAЧе
өЪИэЦЬЖЪЈ¬өЪVIIAЧе
Ј®
ЈЁ2Ј©AФӘЛШУлЛ®·ҙУҰөДАлЧУ·ҪіМКҪКЗ
2Na+2H2O=2Na++2OH-+H2Ўь
2Na+2H2O=2Na++2OH-+H2Ўь
Ј®
ЈЁ3Ј©РҙіцCФӘЛШөДөҘЦКҙУAЎўBБҪФӘЛШЧйіЙөД»ҜәПОпөДЛ®ИЬТәЦРЦГ»»іцBФӘЛШөДөҘЦКөД»ҜС§·ҪіМКҪ
Cl2+Na2S=2NaCl+SЎэ
Cl2+Na2S=2NaCl+SЎэ
Ј®
ЈЁ4Ј©BD
2әНC
2ҫщҫЯУРЖҜ°ЧРФЈ¬¶юХЯөДЖҜ°ЧФӯАн
І»Н¬
І»Н¬
Ј®ЈЁМоЎ°ПаН¬Ўұ»тЎ°І»Н¬ЎұЈ©
ЈЁ5Ј©BФӘЛШөДөҘЦКФЪІ»Н¬өДМхјюПВҝЙТФУлO
2·ўЙъТ»ПөБР·ҙУҰЈә
BЈЁsЈ©+O
2=BO
2ЈЁgЈ©Ј»ЎчH=-296.8kj?mol
-12BD
2ЈЁsЈ©+O
2ЈЁgЈ©

2BO
3ЈЁgЈ©Ј»ЎчH=-196.6kJ?mol
-1Фт1mol BO
3ЈЁgЈ©ИфНкИ«·ЦҪвіЙBЈЁsЈ©Ј¬·ҙУҰ№эіМЦРөДИИР§УҰОӘ
ЎчH=+395.1kJ/mol
ЎчH=+395.1kJ/mol
Ј®
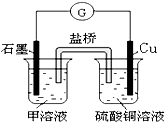
ЈЁ6Ј©ЗвСхИјБПөзіШДЬБҝЧӘ»ҜВКёЯЈ¬ҫЯУР№гА«өД·ўХ№З°ҫ°Ј®ИзНјЈЁ1Ј©ЛщКҫЈ¬өзіШЦРХэј«өДөзј«·ҙУҰКҪОӘ
O2+2H20+4e-=4OH-
O2+2H20+4e-=4OH-
Ј®
ЈЁ7Ј©ЗвЖшКЗәПіЙ°ұөДЦШТӘФӯБПЈ¬әПіЙ°ұ·ҙУҰөДИИ»ҜС§·ҪіМКҪИзПВЈә
N
2ЈЁgЈ©+3H
2ЈЁgЈ©

2NGH
3ЈЁgЈ©Ј»ЎчH=-92.4kJ/mol

ўЩөұәПіЙ°ұ·ҙУҰҙпөҪЖҪәвәуЈ¬ёДұдДіТ»НвҪзМхјюЈЁІ»ёДұдN
2ЎўH
2әНNH
3өДБҝЈ©Ј¬·ҙУҰЛЩВКУлКұјдөД№ШПөИзНјЈЁ2Ј©ЛщКҫЈ®НјЦРt
1КұТэЖрЖҪәвТЖ¶ҜөДМхјюҝЙДЬКЗ
јУС№
јУС№
Ј®ЖдЦРұнКҫЖҪәв»мәПОпЦРNH
3өДә¬БҝЧоёЯөДТ»¶ОКұјдКЗ
t2-t3
t2-t3
Ј®
ўЪОВ¶ИОӘTЎжКұЈ¬Ҫ«2a molH
2әНa molN
2·ЕИл0.5LГЬұХИЭЖчЦРЈ¬ід·Ц·ҙУҰәуІвөГN
2өДЧӘ»ҜВКОӘ50%Ј®ФтёГ·ҙУҰөДЖҪәвіЈКэОӘ
Ј®

 2BO3ЈЁgЈ©Ј»ЎчH=-196.6kJ?mol-1
2BO3ЈЁgЈ©Ј»ЎчH=-196.6kJ?mol-1 2NGH3ЈЁgЈ©Ј»ЎчH=-92.4kJ/mol
2NGH3ЈЁgЈ©Ј»ЎчH=-92.4kJ/mol


 NH4++OH-
NH4++OH- NH4++OH-
NH4++OH-