
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
ЈЁұҫМв№І12·ЦЈ©Ҫ«ҙҝРҝЖ¬әНҙҝНӯЖ¬°ҙНј·ҪКҪІеИл100 mLПаН¬ЕЁ¶ИөДПЎБтЛбЦРТ»¶ОКұјдЈ¬»ШҙрПВБРОКМвЈә
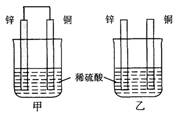
ЈЁ1Ј©ПВБРЛө·ЁХэИ·өДКЗ____________ЎЈ
AЈ®јЧЎўТТҫщОӘ»ҜС§ДЬЧӘұдОӘөзДЬөДЧ°ЦГ
BЈ®ТТЦРНӯЖ¬ЙПГ»УРГчПФұд»Ҝ
CЈ®јЧЦРНӯЖ¬ЦКБҝјхЙЩЎўТТЦРРҝЖ¬ЦКБҝјхЙЩ
DЈ®БҪЙХұӯЦРИЬТәөДc(H+)ҫщФцРЎ
ЈЁ2Ј©ФЪПаН¬КұјдДЪЈ¬БҪЙХұӯЦРІъЙъЖшЕЭөДЛЩ¶ИЈәјЧ____ТТЈЁМоЎ°ЈҫЎұЎўЎ°ЈјЎ°»тЎ°ЈҪЎұЈ©ЎЈ
ЈЁ3Ј©өұјЧЦРІъЙъ1.12LЈЁұкЧјЧҙҝцЈ©ЖшМеКұЈ¬НЁ№эөјПЯөДөзЧУКэДҝОӘ_______________ЎЈ
ЈЁ4Ј©өұТТЦРІъЙъ1.12LЈЁұкЧјЧҙҝцЈ©ЖшМеКұЈ¬Ҫ«РҝЎўНӯЖ¬ИЎіцЈ¬ФЩҪ«ЙХұӯЦРөДИЬТәПЎКНЦБ1 LЈ¬ІвөГИЬТәЦРc(HЈ«)ЈҪ0.1 molЎӨLЈӯ1ЈЁЙи·ҙУҰЗ°әуИЬТәМе»эІ»ұдЈ©ЎЈКФИ·¶ЁФӯПЎБтЛбөДОпЦКөДБҝЕЁ¶ИОӘ_________________ЎЈ
(5) јЧЦРРҝЖ¬ЙП·ўЙъөДөзј«·ҙУҰЈә _________________________Ј»
(6) ИфјЧЦРБҪөзј«өДЧЬЦКБҝОӘ60 gЈ¬№ӨЧчТ»¶ОКұјдәуЈ¬ИЎіцРҝЖ¬әННӯЖ¬Пҙҫ»ёЙФпәуіЖЦШЈ¬ЧЬЦКБҝОӘ47 gЈ¬ФтЈәЗвЖшөДМе»э(ұкЧјЧҙҝц)ОӘ________ЎЈ
ЈЁ12·Ц
Ді»ҜС§·ҙУҰ2A(g)  B(g)+D(g)ФЪЛДЦЦІ»Н¬МхјюПВҪшРРЈ¬·ҙУҰЖчҫщОӘПаН¬әгИЭГЬұХИЭЖчЈ¬BЎўDЖрКјЕЁ¶ИОӘ0ЎЈ·ҙУҰОпAөДЕЁ¶ИЈЁmolЎӨL−1Ј©Лж·ҙУҰКұјдЈЁminЈ©өДұд»ҜЗйҝцИзПВұнЈә
B(g)+D(g)ФЪЛДЦЦІ»Н¬МхјюПВҪшРРЈ¬·ҙУҰЖчҫщОӘПаН¬әгИЭГЬұХИЭЖчЈ¬BЎўDЖрКјЕЁ¶ИОӘ0ЎЈ·ҙУҰОпAөДЕЁ¶ИЈЁmolЎӨL−1Ј©Лж·ҙУҰКұјдЈЁminЈ©өДұд»ҜЗйҝцИзПВұнЈә

ёщҫЭЙПКцКэҫЭЈ¬НкіЙПВБРМоҝХ:
ЈЁ1Ј©ФЪКөСй1ЦРЈ¬·ҙУҰФЪ10ЦБ20·ЦЦУКұјдДЪЖҪҫщЛЩВКОӘ ЎЈ
ЈЁ2Ј©ФЪКөСй2ЦРЈ¬AөДіхКјЕЁ¶Иc 2= molЎӨL−1Ј¬·ҙУҰҫӯ20·ЦЦУҫНҙпөҪЖҪәвЈ¬ҝЙНЖІвКөСй2ЦР»№Тюә¬өДМхјюКЗ ЎЈ
ЈЁ3Ј©ЙиКөСй3өД·ҙУҰЛЩВКОӘҰФ3Ј¬КөСй1өД·ҙУҰЛЩВКОӘҰФ1Ј¬ФтҰФ3 ҰФ1ЈЁМо>Ўў=Ўў<Ј©Ј¬ЗТc 3= ЎЈ
ЈЁ4Ј©УЙұҫҙОКөСйЈ¬ҝЙНЖІвёГ·ҙУҰКЗ ·ҙУҰЈЁСЎМоОьИИ»т·ЕИИЈ©ЎЈАнУЙКЗЈә ЎЈ
ЈЁ5Ј©1Ў«4ЧйКөСйЦРЈ¬AөДЖҪәвЧӘ»ҜВКЧоҙуөДКЗөЪ ЧйЎЈ[АҙФҙ:Zxxk.Com]
ЈЁ6Ј©ФЪКөСй2ЦРЈ¬50 minәуЈ¬ИфҪ«ИЭЖчМе»эФцҙу1ұ¶Ј¬ФтҙпЖҪәвКұBөДЕЁ¶ИОӘ Ј»ёГ·ҙУҰөДЖҪәвіЈКэK ЈЁМоЎ°І»ұдЎұЎўЎ°ФцҙуЎұ»тЎ°јхРЎЎұЈ©ЎЈ
(12·Ц)ЈЁ1Ј©Ў°жП¶рТ»әЕЎұөЗФВіЙ№ҰЈ¬КөПЦБЛЦР№ъИЛЎ°ұјФВЎұөДГОПлЈ®Ў°жП¶рТ»әЕЎұК№УГөДНЖҪшјБКЗТәЗвәНТәСхЈ¬ХвЦЦНЖҪшјБөДУЕөгКЗПаН¬ЦКБҝКұЈ¬ЗвЖш·ЕіцөДИИБҝ¶аЈ¬ІъОпОӘЛ®ОЮОЫИҫЎЈ
ТСЦӘЈәH2(g)Ј«O2(g)=H2O(l)ЎЎҰӨH=Јӯ285.8 kJ/mol ; H2(g)=H2(l)ЎЎҰӨH=Јӯ0.92 kJ/mol
O2(g)=O2(l)ЎЎҰӨHЈҪЈӯ6.84 kJ/mol ; H2O(l)=H2O(g)ЎЎҰӨHЈҪЈ«44.0 kJ/mol
ЗлРҙіцТәЗвәНТәСхЙъіЙЖшМ¬Л®өДИИ»ҜС§·ҪіМКҪЈә_______________________________.
ЈЁ2Ј©ТСЦӘЈәўЩNH3(g)Ј«HCl(g)===NH4Cl(s) ҰӨHЈҪЈӯ176 kJ/mol
ўЪNH3(g)Ј«H2O(l)===NH3ЎӨH2O(aq) ҰӨHЈҪЈӯ35.1 kJ/mol
ўЫHCl(g)===HCl(aq)ЎЎ ҰӨHЈҪ Јӯ72.3 kJ/mol
ўЬNH3ЎӨH2O(aq)Ј«HCl(aq)===NH4Cl(aq)Ј«H2O(l) ҰӨHЈҪЈӯ52.3 kJ/mol
ФтNH4Cl(s)===NH4Cl(aq)өДҰӨHЈҪ______
ЈЁ3Ј©·ЦұрИЎ40 mLөД0.50 mol/LСОЛбУл0.55 mol/LЗвСх»ҜДЖИЬТәҪшРРЦРәН·ҙУҰЈ®НЁ№эІв¶Ё·ҙУҰ№эіМЦРЛщ·ЕіцөДИИБҝҝЙјЖЛгЦРәНИИЈ®Зл»ШҙрПВБРОКМвЈ®
ўЩ АнВЫЙППЎЗҝЛбЎўПЎЗҝјо·ҙУҰЙъіЙ1 molЛ®Кұ·Еіц57.3 kJөДИИБҝЈ¬РҙіцұнКҫПЎБтЛбәНПЎЗвСх»ҜДЖИЬТә·ҙУҰөДЦРәНИИөДИИ»ҜС§·ҪіМКҪ __
ўЪ јЩЙиСОЛбәНЗвСх»ҜДЖИЬТәөДГЬ¶И¶јКЗ1 g/cm3Ј¬УЦЦӘЦРәНәуЙъіЙИЬТәөДұИИИИЭ
cЈҪ4.18 J/(gЎӨЎж)Ј®ОӘБЛјЖЛгЦРәНИИЈ¬КөСйКұ»№РиІвБҝөДКэҫЭУР(МоРтәЕ)__________Ј»
| AЈ®·ҙУҰЗ°СОЛбИЬТәөДОВ¶И | BЈ®·ҙУҰЗ°СОЛбИЬТәөДЦКБҝ |
| CЈ®·ҙУҰЗ°ЗвСх»ҜДЖИЬТәөДОВ¶И | DЈ®·ҙУҰЗ°ЗвСх»ҜДЖИЬТәөДЦКБҝ |
| КөСй РтәЕ | ЖрКјОВ¶Иt1/Ўж | ЦХЦ№ОВ¶Иt2/Ўж | |
| СОЛб | ЗвСх»ҜДЖ | »мәПИЬТә | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
(12·Ц)¶МЦЬЖЪЦчЧеФӘЛШAЎўBЎўCЎўDЎўEФЪФӘЛШЦЬЖЪұнЦРөДО»ЦГИзПВНјЛщКҫЈә
| | B | C | D | |
| A | | E | ||
(12·Ц)ТФБтМъҝуОӘФӯБПЙъІъБтЛбЛщөГөДЛбРФ·ПЛ®ЦРЙйФӘЛШә¬Бҝј«ёЯЈ¬ОӘҝШЦЖЙйөДЕЕ·ЕЈ¬ІЙУГ»ҜС§іБҪө·ЁҙҰАнә¬Йй·ПЛ®Ј¬Па№ШКэҫЭИзПВұнЎЈ

ұн1Ј®јёЦЦЙйЛбСОөДKsp ұн2Ј®№Өі§ОЫИҫОпЕЕ·ЕЕЁ¶Иј°ФКРнЕЕ·ЕұкЧј
»ШҙрТФПВОКМвЈә
ўЕёГБтЛб№Өі§ЕЕ·ЕөД·ПЛ®ЦРБтЛбөДОпЦКөДБҝЕЁ¶Иc(H2SO4)ЈҪ______________molЎӨLЈӯ1ЎЈ
ўЖРҙіцДСИЬОпCa3(AsO4)2өДKspұнҙпКҪЈәKsp[Ca3(AsO4)2]ЈҪ______________Ј¬Иф»мәПИЬТә
ЦРAl3Ј«ЎўFe3Ј«өДЕЁ¶ИҫщОӘ1.0ЎБ10Јӯ4molЎӨLЈӯ1Ј¬c(AsO43Јӯ)өДЧоҙуКЗ_______________molЎӨLЈӯ1ЎЈ
ўЗ№Өі§ЕЕ·ЕіцөДЛбРФ·ПЛ®ЦРөДИэјЫЙйЈЁH3AsO3ИхЛбЈ©І»ТЧіБҪөЈ¬ҝЙН¶ИлMnO2ПИҪ«ЖдСх»ҜіЙОејЫЙйЈЁH3AsO4ИхЛбЈ©Ј¬РҙіцёГ·ҙУҰөДАлЧУ·ҪіМКҪ_________________________ЎЈ
ўИФЪҙҰАнә¬Йй·ПЛ®КұІЙУГ·Ц¶ОКҪЈ¬ПИПт·ПЛ®ЦРН¶ИлЙъКҜ»ТөчҪЪpHөҪ2Ј¬ФЩН¶ИлЙъКҜ»ТҪ«pHөчҪЪөҪ8ЧуУТК№ОејЫЙйТФCa3(AsO4)2РОКҪіБҪөЎЈ
ўЩҪ«pHөчҪЪөҪ2Кұ·ПЛ®ЦРУРҙуБҝіБөнІъЙъЈ¬іБөнЦчТӘіЙ·ЦөД»ҜС§КҪОӘ______________Ј»
ўЪCa3(AsO4)2ФЪpHөчҪЪөҪ8ЧуУТІЕҝӘКјіБөнөДФӯТтОӘ_____________________________ЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com