
题目列表(包括答案和解析)

| 点燃 |
| 点燃 |
| 1 |
| 5 |
| 1 |
| 5 |

| ||
| ||
有关空气中氧气体积分数的探究
(1)
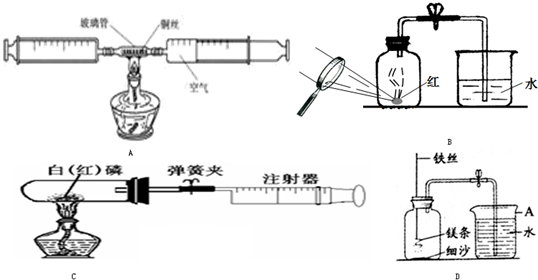
小明同学为了测定空气中氧气和氮气的体积分数,设计了以下实验:①用一定量的空气和足量的铜粉在加热条件下充分反应,然后在同样条件下测定反应后得到的气体的体积.
②用一定量的空气和足量的碳粉在加热条件下充分反应.然后在同样条件下测定反应后得到的气体的体积.
③在密闭容器中充人一定量的空气,让小动物在容器中充分呼吸,然后在同样条件下测定所剩余的气体的体积.
其中可以比较准确地测定出空气中氧气和氮气的体积分数的实验是
________.其理由________.如图是李华和黄磊两位同学设计的测定空气中氧气体积分数的实验装置.

①这两位学生在燃烧匙内加入的可燃物应该是
________.②若李华同学的实验操作准确无误,燃烧停止并冷却后,打开止水夹,瓶内进水的体积约为
________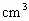 .
.
③黄磊同学因操作不当,瓶内进水体积比李华同学略小.请分析:黄磊同学产生实验误差的原因可能是下列选项中的
________(填序号):|
A .燃烧匙内可燃物的量不足 |
B .燃烧匙内可燃物有剩余 |
|
C .气密性不好 |
D .未冷却至室温就打开止水夹 |
|
E .导管太长 |
舒畅同学为测定空气中氧气所占的体积分数,设计了如图所示的实验:在一个耐热活塞的底部放一小块
(足量)白磷,然后迅速将活塞下压,可以观察到的现象是________;
冷却至原来温度时,慢慢松开手,活塞最终将回到刻度
________处,试简述白磷燃烧的原因________.| 反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
| 25mL | 22mL |
| 1 |
| 5 |
| 1 |
| 5 |
| 加热 |
| 加热 |
| 反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
| 25mL | 22mL |
| 1 |
| 5 |
| 1 |
| 5 |
| 点燃 |
| 点燃 |
| 点燃 |
| 点燃 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com