化学实验室的开放日,老师安排化学兴趣小组的同学开展了有关NaCl和Na
2CO
3这两种常见的盐的实验,实验任务如下:
第一小组的同学:将失去标签的两瓶无色溶液(分别为NaCl和Na
2CO
3)区别开来
第二小组的同学:除去NaCl固体中的少量Na
2CO
3第三小组的同学:测定Na
2CO
3和少量NaCl的固体混合物中Na
2CO
3质量分数
(1)第一小组的同学为了区别两瓶无色溶液,甲、乙、丙、丁四位同学分别选择下列物质进行实验.其中合理的是______(填写序号).
甲:稀盐酸 乙:AgNO
3溶液 丙:澄清石灰水 丁:蓝色的石蕊试纸
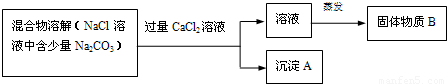
(2)第二小组为了除去NaCl溶液中的少量Na
2CO
3,设计了如下的实验:
请回答下列问题:
①写出沉淀A的化学式______;②甲同学认为:加入CaCl
2溶液后,分离除去沉淀A的实验操作方法是______;③乙同学发现此方案很容易引入新的杂质,他们提出新的方案:将混合物溶解,若滴加盐酸至不再产生气体为止,则既能除去Na
2CO
3杂质,又能有效地防止新杂质的引入.写出有关反应的方程式______.
(3)第三小组的同学根据下列所给出的药品、实验装置和实验中可测得的数据,设计实验来粗略测定Na
2CO
3和NaCl的固体混合物ag中Na
2CO
3的质量分数.
药品:足量的稀H
2SO
4、CaCl
2溶液、碱石灰(烧碱和氧化钙的混合物)、浓硫酸
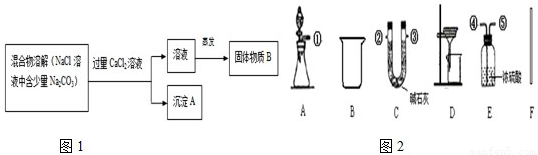
实验装置如图2:
在实验中可测得的数据:①充分反应后,生成沉淀的质量为bg; ②反应前装置和药品的质量为c g;③充分反应后装置和药品的质量为d g.
请设计二个实验方案填入下表中(碱石灰和浓硫酸已被选用,下表中不再填写):
| 方案 | 选用的药品 | 选用的实验装置及组装时接口连接顺序 | 需测得的实验数据(从上述可测得的数据中选取) | 混合物中Na2CO3的质量分数计算式 |
| 选用的实验装置序号 | 组装时接口编号顺序 |
| 一 | ______ | A、B、D、F | (毋须填写) | ______ | ______ |
| 二 | ______ | ______ | ______ | ag、cg、dg | ______ |