
题目列表(包括答案和解析)
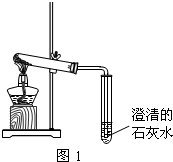 含钠元素、钙元素的化合物是初中化学的重要研究对象之一.
含钠元素、钙元素的化合物是初中化学的重要研究对象之一.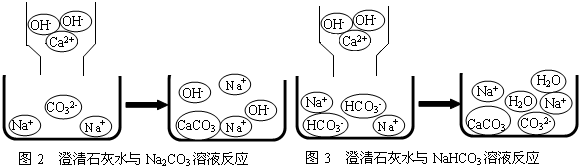
| 实验内容 | 实验现象 | 实验结论 |
| 方案一:取少量滤液加入试 管中,向其中 |
娇娇同学的猜想是正确的. 滤液中含有的两种溶质是 | |
| 方案二:取少量滤液加入试管中,向其中 |
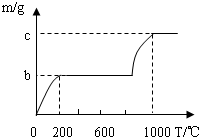 学们认为实验过程中产生的废液必须处理后再排放.请你对B试管中滤液的处理提出可行的建议
学们认为实验过程中产生的废液必须处理后再排放.请你对B试管中滤液的处理提出可行的建议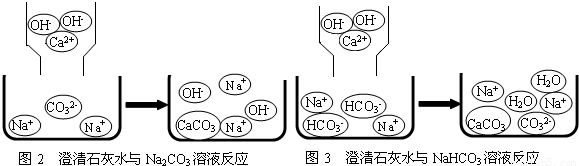
| 实验内容 | 实验现象 | 实验结论 |
| 方案一:取少量滤液加入试 管中,向其中______ | ______ | 娇娇同学的猜想是正确的. 滤液中含有的两种溶质是 ______ |
| 方案二:取少量滤液加入试管中,向其中______ | ______ |
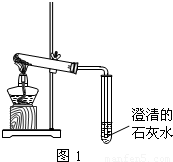
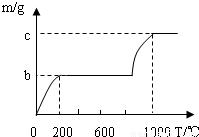
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 取四支试管,各取少量的A、B、C、D溶液,分别先滴加紫色石蕊试液 | B溶液变红色,D溶液变成蓝色.A、C溶液都呈________色. | B 是________; D 是________ |
| 2 | 另取两支试管,各取少量的A、C溶液,分别滴加硝酸钡后再滴入稀硝酸溶液. | A________. C________. | A是硫酸钠溶液 C是________ |
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 3 | 取该溶液少量试管E中,加入硝酸钡溶液后再加入稀硝酸 | 有白色沉淀生成 | 不能确定猜想________一定成立 |
| 4 | 取该溶液少量试管F中,加入稀盐酸,加热 | 有刺激性气味的气体生成 | 猜想________可能成立 |
| 5 | 所得溶液中加入足量的________ | ________ | 猜想(3)成立 |
| 某实验小组对实验室中A、B、C、D四瓶无色溶液进行鉴别,它们分别是硫酸钠、稀硫酸、澄清石灰水、氯化钠四种物质的一种。可供使用的实验用品有:稀盐酸、稀硫酸、碳酸钠、紫色石蕊溶液、硝酸钡溶液、硝酸银溶液、稀硝酸溶液、玻璃棒、试管、胶头滴管。 (一)请利用提供的实验用品,鉴别出四种物质,并完成实验报告: | ||||||||||||||||
SO42-时,亚硫酸根离子(SO32-)的存在干扰了SO42-的检验。如往亚硫酸钠(Na2SO3)溶液滴加硝酸钡溶液后有沉淀生成,再加足量的稀硝酸酸依然有白色沉淀。 【提出问题】若某无色溶液中可能含有硫酸根离子(SO42-)与亚硫酸根离子(SO32-)中的一种或两种,该如何检验? 【查阅资料】亚硫酸钡(Ba2SO3)是无色晶体或白色粉末,微溶于水,在水中是白色沉淀。中性或碱性条件下NO3-不能和SO32-反应,但在酸性条件下,NO3-能和H+反应相遇时(HNO3)具有强氧化性,易把SO32-氧化生成SO42-。往亚硫酸钡中加入盐酸能发生类似于碳酸钡与盐酸的反应,生成有刺激性的气体。 (二)【猜 想】该无色溶液中含有(1)SO42- (2)SO32- (3) 。 【实验探究】请你将下列实验填写完整。 | ||||||||||||||||
【得出结论】要鉴别一种离子的存在,必须排除其它离子的干扰,不然会得出错误的结论。 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com