
题目列表(包括答案和解析)
| A、原子核和核外电子 | B、质子和中子 | C、中子和电子 | D、电子和质子 |


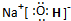
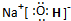
A、 B、C、D 四种元素, A B C的电子层数之和为5,A B能形成AB3分子,C元素的最高正价与其最低负价的绝对值相等,D的最外层电子数是次外层电子数的3倍。
(1)某物质含有上述四种元素中的2种,其空间构型为正四面体,该微粒的化学式为_____
(2)某盐含有上述四种元素,其水溶液显酸性。它与NaOH以物质的量之比(下同)1:1反应时无气体产生,1:2时能产生气体。该盐与盐酸反应生成含2个碳原子的酸,写出该盐的化学式___________ 。写出该盐与与NaOH以物质的量之比1:2反应的离子方程式 ___________ 。用方程式解释该盐水溶液显酸性的原因?__________________________________________。
A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。A元素的一种核素质子数与质量数在数值上相等;B、E同主族,且核电荷数之比为1︰2;C的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子;D的最外层电子数是内层电子总数的一半。试回答下列问题:
(1)F位于周期表中第________周期________族。
(2)常温时,39 g B、C按原子个数比1︰l形成的化合物X与足量CO2反应放出Q kJ的热量,写出该反应的热化学方程式 ;
写出少量X与FeCl2溶液反应的离子方程式_______________________________________。
(3)B、C、F组成的化合物Y是家用消毒剂的主要成分,Y的溶液呈碱性,用离子方程式解释其原因______________________________;起消毒作用的微粒电子式为_________。
(4)四原子分子Z与C的单质和水反应所得的阴离子电子数相等,Z的分子空间构型为___________型,它属于_________分子(填“极性”或“非极性”);请比较Z与DA3的沸点高低并加以解释_____________________________________________________。
(5)目前人们正在研究开发一种高能电池,它是以熔融的C、E单质为两极,以C离
子导电的β-Al2O3陶瓷作固体电解质,反应式为:2C+xE ![]() C2Ex 。请写出电池放电时正负极的电极反应式,正极反应式:_______________________。用该电池作电源进行电解含有0.2 mol CuSO4和0.2 mol NaCl的混合溶液500 mL时:若此电池工作一段时间后消耗23 g C单质 。则阳极产生气体体积为:________L(标准状况下);电解后溶液加水稀释至2 L ,溶液的pH为:________。
C2Ex 。请写出电池放电时正负极的电极反应式,正极反应式:_______________________。用该电池作电源进行电解含有0.2 mol CuSO4和0.2 mol NaCl的混合溶液500 mL时:若此电池工作一段时间后消耗23 g C单质 。则阳极产生气体体积为:________L(标准状况下);电解后溶液加水稀释至2 L ,溶液的pH为:________。
A、B、C、D、E五种微粒,它们可能是原子或离子,并且所含的元素都在短周期。A显负价时,不能被任何氧化剂氧化;金属B的原子核内质子数比前一周期的同族元素多8,其单质不能从CuSO4溶液中置换出Cu;C元素有三种同位素,Cl、C2、C3,C1的质量数分别为C2、C3的1/2和1/3;D的气态氢化物溶于水后显碱性;E是由两种不同元素组成的带负电荷的微粒,它共有10个电子,E极易与C+结合成中性微粒。回答:
(1)写出五种微粒的符号:A 、B 、C 、D 、E 。
(2)C的同位素名称:C2 。
(3)C和D形成分子的电子式为 ,空间结构为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com