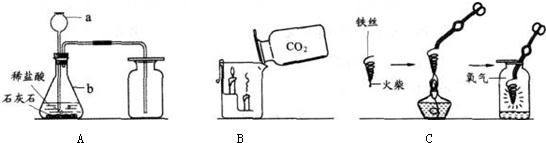
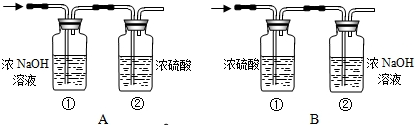
化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图(如图1)回答问题:
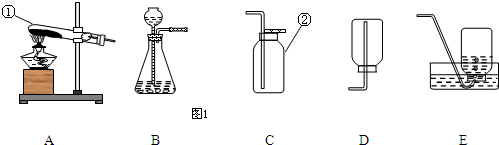
(1)写出指定仪器的名称:①
试管
试管
②
集气瓶
集气瓶
(2)下面四种途径都可以得到氧气(如图2):
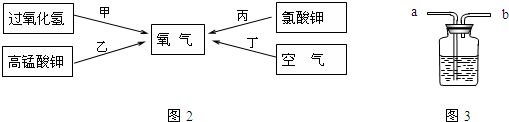
写出实验室中通过甲、乙两种途径制取氧气的文字表达式甲
乙
(3)化学实验的绿色化就是以绿色化学的理念和原则来指导实验工作.从实现原料和反应过程的绿色化考虑,你认为在中学化学实验室中,甲、乙、丙、三种制取氧气的途径中,
甲
甲
(填“甲”或“乙”或“丙”或“丁”)途径更体现化学实验的绿色化追求.
(4)实验室用高锰酸钾制取氧气时,可选用的发生装置是
A
A
(填字母代号).用排水收集氧气完毕后,停止加热时的操作顺序是先
撤出导管
撤出导管
,然后
熄灭酒精灯
熄灭酒精灯
,以防止水倒吸进入热的试管中,造成试管破裂.
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH
3是一种无色、有刺激性气味的气体,密度比空气小.NH
3极易溶于水,其水溶液呈碱性.现选择合适的装置
来制取并收集NH
3,应该选择的发生装置是
A
A
,收集装置是
D
D
.
我认为选择气体收集方法,从气体性质的角度需要考虑的因素是:
气体的密度
气体的密度
.
溶水性
溶水性
(6)汽车尾气中的一氧化氮是一种大气污染物.它是一种无色气体,难溶于水,密度比
空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮气体.实验室中制取一氧化氮采用的收集装置是(填序号)
E
E
.
(7)在医院里给病人输氧时,在氧气钢瓶和病人吸氧器之间连接一个类似如图3所示的装置,在装置中盛放大约半瓶蒸馏水,导气管
a
a
(填“a”或“b”)端连接在供氧气的钢瓶上,该装置的作用有(填写一条)
观察氧气的流速
观察氧气的流速
.