(1)如图1,横坐标为溶液的pH,纵标为金属离子的物质的量浓度的对数(当溶液中金属离子浓度≤10
-5mol?L
-1时,可认为沉淀完全).试回答下列问题:

①腐蚀铜板后的溶液中,若Cu
2+、Fe
3+和Fe
2+浓度均为0.1mol?L
-1,今向混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为
②从图1中数据计算可得Fe(OH)
2的溶度积K
sp[Fe(OH)
2]=
(2)25℃时,测得浓度为0.1mol?L
-1的HA溶液的pH=3,则HA的电离常数K
a=
(3)固定和利用CO
2能有效地利用资源,并减少空气中的温室气体.工业上有一种用CO
2来生产甲醇燃料的方法:CO
2(g)+3H
2(g)?CH
3OH(g)+H
2O(g)△H=-49.0kJ?mol
-1某科学实验将6molCO
2和8molH
2充入2L密闭容器中,测得H
2的物质的量随时间变化如2图所示(实线).图中数据a(1,6)代表的意思是:在1 min时H
2的物质的量是6mol.
①下列时间段平均反应速率最大的是
,最小的是
.
A.0-1min B.1-3min C.3-8min D.8-11min
②仅改变某一实验条件再进行两次实验测得H
2的物质的量随时间变化如图2中虚线所示,曲线Ⅰ对应的实验改变的条件是
,曲线Ⅱ对应的实验改变的条件是
.
③根据该反应特点,此反应自发进行的条件是
(填“高温”、“低温”或“任何温度”).
(4)铁是一种廉价的金属,除了做为重要的结构材料外,现又有了新的用途,磷酸聚合物铁锂电池以其廉价、高容量和安全性逐渐占据市场.高铁电池的研究也在进行中.下图是高铁电池的实验装置:
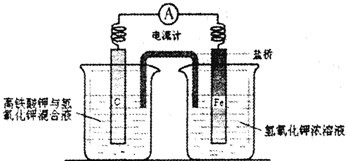
已知放电后,两极反应均生成Fe的+3价的化合物.
①该电池放电时正极发生的电极反应是
.
②若该电池属于二次电池,则充电时阴极反应的电极反应式为
.

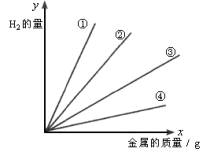
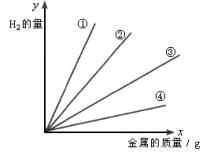


 如图所示为电解质溶液的PH随外界条件T变化的图象,下列的叙述不正确的是( )
如图所示为电解质溶液的PH随外界条件T变化的图象,下列的叙述不正确的是( )