
题目列表(包括答案和解析)
某学生测定CuSO4· H2O晶体的
H2O晶体的 值,数据如下(已知
值,数据如下(已知 的理论值为5.0):
的理论值为5.0):
|
坩埚质量 |
坩埚+试样 |
失水后坩埚+试样 |
|
11.700g |
14.200g |
13.201g |
产生误差的可能原因是
A.硫酸铜晶体中含不挥发杂质 B.未放人干燥器中冷却
C.实验前,晶体有吸附水 D.未做恒重操作
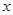 H2O晶体的
H2O晶体的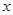 值,数据如下(已知
值,数据如下(已知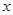 的理论值为5.0):
的理论值为5.0):| 坩埚质量 | 坩埚+试样 | 失水后坩埚+试样 |
| 11.700g | 14.200g | 13.201g |
某学生测定CuSO4·![]() H2O晶体的
H2O晶体的![]() 值,数据如下(已知
值,数据如下(已知![]() 的理论值为5.0):
的理论值为5.0):
| 坩埚质量 | 坩埚+试样 | 失水后坩埚+试样 |
| 11.700g | 14.200g | 13.201g |
产生误差的可能原因是
A.硫酸铜晶体中含不挥发杂质 B.未放人干燥器中冷却
C.实验前,晶体有吸附水 D.未做恒重操作
某学生测定CuSO4· H2O晶体的
H2O晶体的 值,数据如下(已知
值,数据如下(已知 的理论值为5.0):
的理论值为5.0):
| 坩埚质量 | 坩埚+试样 | 失水后坩埚+试样 |
| 11.700g | 14.200g | 13.201g |
| |||||||||||||||||||||||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com