
题目列表(包括答案和解析)
| 元素 | A | B | C | D | E |
| 性质 结构 信息 |
室温下单质呈粉末状固体,加热易熔化,是黑火药的成分之一. 单质在氧气中燃烧,发出明亮的蓝紫色火焰. |
单质常温、常压下是黄绿色气体,能溶于水. | 单质质软、银白色固体、导电性强. 单质在空气中燃烧发出黄色的火焰. |
是形成化合物最多的元素,其单质有多种同素异形体 | 单质导电性良好,其氧化物和最高价氧化物的水化物都具有两性. |





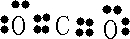
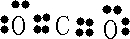
 H++Cl-+HClO
H++Cl-+HClO H++Cl-+HClO
H++Cl-+HClO
| 元素符号 | 元素性质或结构信息 |
| A | 原子核外L层未成对电子数最多 |
| B | 原子半径是短周期主族元素中最大的 |
| C | 地壳中含量最多的金属元素 |
| D | 原子核外有五种不同能量的电子,且最外层有2对成对电子 |
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。![]()
![]()
![]()
![]()
![]()

![]()
![]()

| 元素 | T | X | Y | Z |
| 性质 结构 信息 | 原子核外s电子总数等于p电子总数;人体内含量最多的元素,且其单质是常见的助燃剂。 | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼 | 单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 | 第三周期元素的简单离子中半径最小 |


 (1)写出元素T的离子结构示意图 ;写出元素X的气态氢化物的电子式 ;写出Z元素原子的核外电子排布式: ;元素Y的原子核外共有______种形状不同的电子云。
(1)写出元素T的离子结构示意图 ;写出元素X的气态氢化物的电子式 ;写出Z元素原子的核外电子排布式: ;元素Y的原子核外共有______种形状不同的电子云。
(2)Z单质与Y最高价氧化物的水化物的水溶液反应的离子方程式
(3)元素T与氟元素相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
a.常温下氟气的颜色比T单质的颜色深 b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。![]()
![]()
![]()
![]()
![]()
![]()
![]()
| 元素 | T | X | Y | Z |
| 性质 结构 信息 | 原子核外s电子总数等于p电子总数;人体内含量最多的元素,且其单质是常见的助燃剂。 | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼 | 单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 | 第三周期元素的简单离子中半径最小 |
(1)写出元素T的离子结构示意图 ;写出元素X的气态氢化物的电子式 ;写出Z元素原子的核外电子排布式: ;元素Y的原子核外共有______种形状不同的电子云。
(2)Z单质与Y最高价氧化物的水化物的水溶液反应的离子方程式
(3)元素T与氟元素相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
a.常温下氟气的颜色比T单质的颜色深 b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com