(Ⅰ)用质量分数为98%的浓硫酸(密度为1.84g/cm
3)配制成1mol/L的稀硫酸.现实验室仅需要这种硫酸220mL.试回答下列问题:
(1)配制稀硫酸时,应选用容量为
250mL
250mL
mL的容量瓶;
(2)经计算需要用量筒量取
13.6
13.6
mL浓硫酸,在量取时宜选用下列量筒中的
C
C
(填字母).
A.5mL B.10mL C.25mL D.50mL
(3)在量取浓硫酸后,进行了下列操作:
①等稀释的硫酸其温度与室温一致后,沿玻璃棒注入容量瓶中.
②往容量瓶中小心加蒸馏水至液面接近环形标线1-2cm处,改用胶头滴管加蒸馏水,使溶液的凹液面底部与瓶颈的环形标线相切.
③将浓硫酸缓缓注入盛适量蒸馏水的烧杯中,并用玻璃棒搅动,使其混合均匀.
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶.
上述操作中,正确的顺序是(填序号)
③①④②
③①④②
.
(4)容量瓶使用之前,检查其是否漏水的具体操作为
用右手食指顶住瓶塞,用左手拖住瓶底,将容量瓶倒转过来看瓶口处是否有水渗出,若没有,将瓶塞旋转180度,重复上述操作,如果瓶口处仍无水渗出,则容量瓶不漏水
用右手食指顶住瓶塞,用左手拖住瓶底,将容量瓶倒转过来看瓶口处是否有水渗出,若没有,将瓶塞旋转180度,重复上述操作,如果瓶口处仍无水渗出,则容量瓶不漏水
.
(5)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓硫酸,其配制的稀硫酸浓度会
偏低
偏低
(填“偏高”、“偏低”、“无影响”).
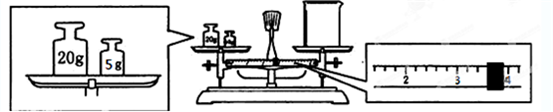
(Ⅱ)某同学称量mgNaOH固体配制V m L 4mol/L的NaOH溶液,下面是该同学配制过程的示意图,其操作中错误的是(填操作序号)
①④⑤
①④⑤
.