
题目列表(包括答案和解析)
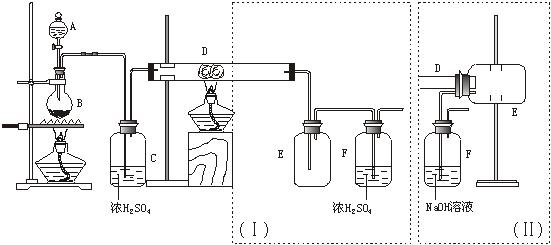 (1)B中反应的化学方程式为: ;
(1)B中反应的化学方程式为: ;
(2)D中的反应开始前,需排除装置中的空气,应采取的方法是:
。
(3)D中反应的化学方程式为: 。
(4)装置(Ⅰ)的主要缺点是: 。
(5)装置(Ⅱ)的主要缺点是: 。
如果选用此装置来完成实验,则必须采取的改进措施是:
。
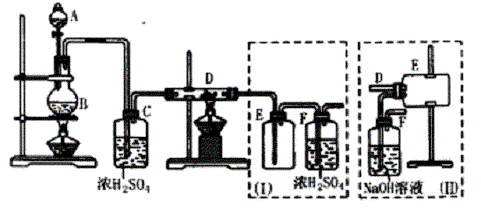
⑴B中反应的化学方程式为 。
⑵D中的反应开始前,需排除装置中的空气,应采取的方法是 。
⑶D中反应的化学方程式为 。
⑷装置(Ⅰ)的主要缺点是 。
⑸装置(Ⅱ)的主要缺点是 。如果选取用此装置来完在实验,则必须采取的改进措施是 。
实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物呈棕红色。易潮解,100℃左右时升华。图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置则不同,分别如(Ⅰ)和(Ⅱ)所示。试回答:
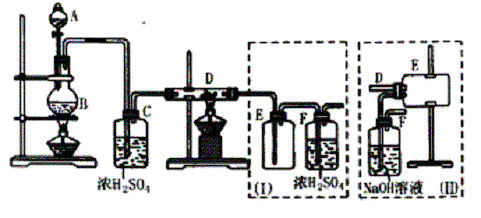
⑴B中反应的化学方程式为 。
⑵D中的反应开始前,需排除装置中的空气,应采取的方法是 。
⑶D中反应的化学方程式为 。
⑷装置(Ⅰ)的主要缺点是 。
⑸装置(Ⅱ)的主要缺点是 。如果选取用此装置来完在实验,则必须采取的改进措施是 。

| ||
| ||
| ||
| ||
实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物呈棕红色、易潮解,100 ℃左右时升华。如下图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置则不同,分别如(Ⅰ)和(Ⅱ)所示。完成下列问题:

(1)B中反应的化学方程式为:__________________________________。
(2)D中反应开始前,需排除装置中的空气,应采取的方法是:__________________________。
(3)D中反应的化学方程式为:__________________________________。
(4)装置(Ⅰ)的主要缺点是:_____________________________________。
(5)装置(Ⅱ)的主要缺点是:_____________________________,如果选用此装置来完成实验,则必须采取的改变措施是:_____________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com