
题目列表(包括答案和解析)
下列关于反应能量的说法正确的是
A.Zn(s) +CuSO4 (aq) =ZnSO4 (aq) +Cu(s) ; △H =—216kJ·mol-1 ,反应物总能量>生成物总能量
B.CaCO3 ( s) = CaO(s) +CO2 (g) ;△H = + 178. 5 kJ·mol-1反应物总能量>生成物总能量
C.l0lkPa 时,2H2 (g)+ O2 (g) =2H2O(1);△H =—571. 6 kJ·mol-1 ,H2的燃烧热为571.6 kJ·mol'
D.H+ (aq) +OH-(aq) =H2O(l) ;△H=—57.3 kJ·mol-' ,含 1molNaOH 的氢氧化钠
溶液与含0.5molH2SO4的浓硫酸混合后放出57.3kJ的热量
下列关于反应能量的说法正确的是
A.Zn(s) +CuSO4 (aq) = ZnSO4 (aq) +Cu(s) ;△H =-216 kJ·mol-1。则反应物总能量 >生成物总能量
B.相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol氢分子的能量为E2。则2E1 = E2
C.l0l kPa时,2H2 (g)+ O2 (g) = 2H2O(1) ;△H =-571.6 kJ·mol-1 ,则H2的燃烧热为571.6 kJ·mol-1
D.H+(aq) +OH-(aq) =H2O(l) ;△H=-57.3 kJ·mol-1 ,含 1 mol NaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量
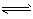 1/2H2(g)+1/2I2(s) △H=26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26. 5kJ的能量
1/2H2(g)+1/2I2(s) △H=26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26. 5kJ的能量 下列关于反应能量的说法正确的是
A.Zn(s) +CuSO4 (aq) = ZnSO4(aq) +Cu(s) ;△H=-216 kJ·mol-1。则反应物总能量>生成物总能量
B.相同条件下,如果1 mol氢原子所具有的能量为E1,1mol氢分子的能量为E2。则2E1 =E2
C.l0l kPa时,2H2(g)+ O2 (g) = 2H2O(1) ;△H =-571.6kJ·mol-1 ,则H2的燃烧热为571.6kJ·mol-1
D.H+(aq) +OH-(aq) =H2O(l) ;△H=-57.3 kJ·mol-1 ,含1 mol NaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com