
题目列表(包括答案和解析)
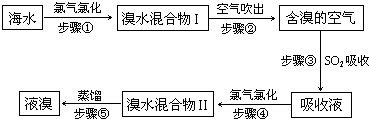
 (2011?宁波模拟)“化学与技术”模块
(2011?宁波模拟)“化学与技术”模块
| ||
| ||
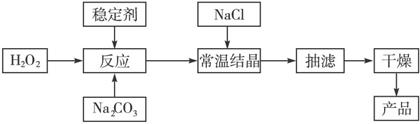
过碳酸钠俗称固体双氧水,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,它的制备原理和路线如下:2Na2CO3+ 3H2O2![]() 2Na2CO3·3H2O2 ΔH<0,回答下列问题:
2Na2CO3·3H2O2 ΔH<0,回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是______________________。
(2)下列物质可使过碳酸钠较快失效的是________________________________。
A.MnO2 B.H2S C.稀硫酸 D.NaHCO3
(3)加入NaCl的作用是________________________________。
(4)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与Fe3+生成稳定的配合物,Fe3+对反应的不良影响是________________________________。
(5)反应的最佳温度控制在15 ℃—
(6)以上生产流程中遗漏了一步,造成所得产品纯度偏低,该步操作的名称是____________。


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com