
题目列表(包括答案和解析)
A、B、C、D均为可溶于水的离子化合物,组成它们的离子有:
| 阳离子 | K+ Fe3+ Al3+ Ba2+ |
| 阴离子 | OH- CO32- SO3 2- NO3- |
分别取它们的水溶液进行实验,结果如下:
①A溶液与适量B溶液反应生成白色沉淀,再加入过量A溶液,沉淀量减少,但不消失;②C溶液与D溶液反应生成有色沉淀:
③B溶液与过量的C溶液反应生成白色沉淀;
请根据上述实验结果,填空:
(1)写出化合物的化学式:A ,B ,C ,D ,
(2)B溶液与过量A溶液反应后,最终得到的沉淀的化学式是 。
(1)C元素的名称是___________。
(2)A、B、D可组成化学式为D4B
(3)B、D形成的化合物液态时可发生微弱电离(电离过程与D
(4)已知:BA2+A2+D![]() DBA3。如图所示,若将一充满m mL BA2和A2混合气体的大试管倒立于D
DBA3。如图所示,若将一充满m mL BA2和A2混合气体的大试管倒立于D

①若余下n mL气体为___________,原混合气体中BA2的体积为___________mL,A2的体积为___________mL。
②若余下n mL气体为___________,原混合气体中BA2的体积为___________mL,A2的体积为___________mL。
A、B、C、D均为短周期元素。A、B可形成两种液态化合物,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。A、B、D可组成离子化合物,该晶体化学式为B4A3D2,其水溶液呈弱酸性。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。已知X分子与B2A分子中的电子数相等。Y分子与最简式为BA的分子中的电子数相等。请回答:
(1)写出元素的名称:A ,C 。
(2)Y分子是 分子(填极性和非极性)。
(3)写出实现下列转化的化学反应方程式并标明电子转移的方向和数目:
C2+(BA)n→A2
(4)B4A3D2水溶液呈酸性,写出其呈酸性的离子方程式:
(14分)A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)。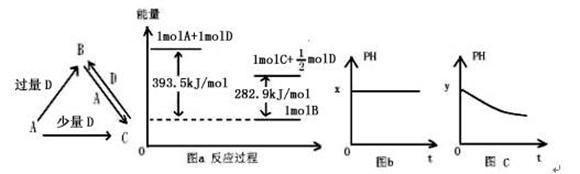
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为 。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则
①C的化学式为 。
②反应B+A→C的离子方程式为 。
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其PH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D为 (填化学式),此时图b中x 7(填“﹥”“﹤”“﹦”)
②若图c符合事实,已知图c中y﹤7,则其PH变化的原因是 (用离子方程式表示)
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com