
题目列表(包括答案和解析)
 O2+Hb·CO 实验表明,c(Hb·CO)即使只有c(Hb·O2)的1/50,也可造成人的智力损伤。已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2mol·L-1,若使c(Hb·CO)小于c(Hb·O2)的1/50,则吸入肺部CO的浓度不能超过_________mol·L-1。
O2+Hb·CO 实验表明,c(Hb·CO)即使只有c(Hb·O2)的1/50,也可造成人的智力损伤。已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2mol·L-1,若使c(Hb·CO)小于c(Hb·O2)的1/50,则吸入肺部CO的浓度不能超过_________mol·L-1。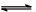 N2(g) + 2CO2(g) △H=-113kJ·mol-1
N2(g) + 2CO2(g) △H=-113kJ·mol-1
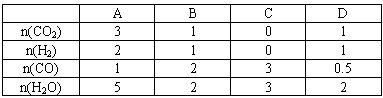
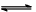 H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表: 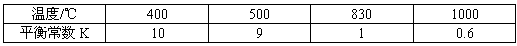
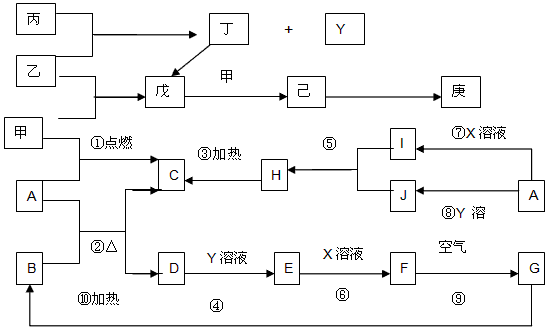
抗氧剂亚硫酸钠可利用硫酸工业的炉气和尾气与纯碱反应来制取,生产流程如下图:

己知:①炉气、尾气中均含有SO2、水蒸气等;②“混合反应”中还溶解有少量Fe2O3、MgO等矿尘。
(1)“混合反应”中纯碱(Na2CO3)参与反应的化学方程式为:
________________ (任写一个)。
(2)用NaOH“除杂”时,主要的离子方程式为:
________ (任写一个)。
(3)通过“操作I”可以得到亚硫酸钠晶体,其操作过程包括:加热蒸发浓缩、
(写出主要步骤名称)及洗涤、干燥。
 (4)硫酸生产中炉气转化反应为:2SO2(g)+O2(g)
(4)硫酸生产中炉气转化反应为:2SO2(g)+O2(g)![]() 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线I所示。
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线I所示。
下列判断正确的是__________(填序号)。
A.该反应的正反应为放热反应
B.曲线I上A、C两点反应速率的关系是:υA>υC
C.反应达到B点时,2υ正(O2)=υ逆(SO3)
D.已知V2O5的催化效果比Fe2O3好,若I表示用V2O5催化剂的曲线,则II是Fe2O3作催化剂的曲线
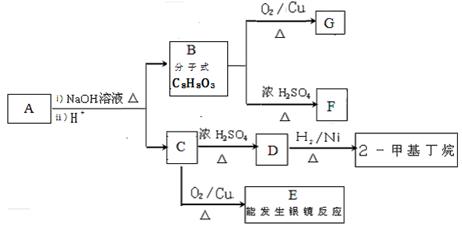
水杨酸己酯分子式为C13H18O3 ,具有花果香味,用作化妆品香料的定香剂,也用作烟草香精。它的一种同分异构体A具有如下转化关系:
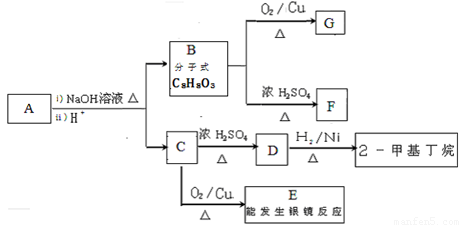
已知:
①C分子中有一个碳原子连接着4个不同的原子或原子团,且1 molC和足量金属Na反应能产生0.5 mol H2
②F中除了含有1个苯环外,还含有1个五元环
(1)写出B的结构简式 ;写出G含有的官能团的名称
(2)写出A和NaOH溶液反应的化学方程式 ;
写出E发生银镜反应的化学方程式 ;
(3)B生成F的反应类型是 ;C生成D的反应类型是 ;
(4)化合物B有多种同分异构体,写出两种符合下列条件的同分异构体的结构简式:
a.属于芳香族化合物
b.酸性条件下能发生水解反应且其中一种产物的苯环上的一氯代物只有两种
c.1 mol该有机物最多可消耗3molNaOH
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com