
题目列表(包括答案和解析)
图中C至L分别表示反应中的一种常见物质,E、F、I在通常情况下是气体单质,其中E有刺激性气味,X、Y是常见的金属单质。W是由甲、乙元素按1∶1的比例组成的,其中甲元素的原子的M层电子数是K层的一半,乙元素的原子最外层电子数是次外层电子数的3倍。(参加反应的水和生成的水已从图中略去)

填写空白:
(1)E是___________(化学式),Y元素在周期表中的位置是______________________。
(2)写出K+G![]() H+J+C的离子方程式________________________________。
H+J+C的离子方程式________________________________。
(3)写出W+L![]() J+C+I的化学方程式_________________________________。
J+C+I的化学方程式_________________________________。
(4)设计实验分离H和J(写出所用试剂和操作方法):_____________________。
图中C至L分别表示反应中的一种常见物质,E、F、I在通常情况下是气体单质,其中E有刺激性气味,X、Y是常见的金属单质.W是由甲、乙元素按1∶1的比例组成的,其中甲元素的原子的M层电子数是K层的一半,乙元素的原子最外层电子数是次外层电子数的3倍.(参加反应的水和生成的水已从图中略去)
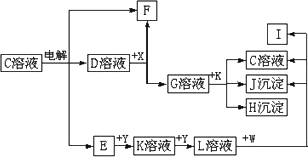
填写空白:
(1)E是________(化学式),Y元素在周期表中的位置是________.
(2)写出K+G→H+J+C的离子方程式________.
(3)写出W+L→J+C+I的化学方程式________.
(4)设计实验分离H和J(写出所用试剂和操作方法):________.
如图中A至L分别表示反应中的一种常见物质,E、F、I在通常情况下是气体单质,其中E有刺激性气体,X、Y是常见的金属单质.W是由甲、乙两种元素按1∶1组成,其中甲元素的原子M层电子数是K层的一半.乙元素的原子最外层电子数是次外层电子数的3倍,参加反应的水和生成的水已从图中略去.
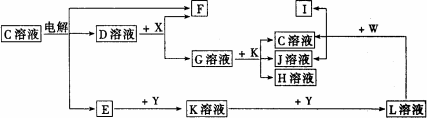
填写下列空白:
(1)E是________(化学式),Y元素在周期表中的位置是____________________.
(2)用电子式表示W的形成过程__________________________.
(3)写出K+G→H+J+C的离子方程式____________________________.
(4)设计实验分离H和J(写出加入试剂和操作方法):_______________.
| 容器 | A | B |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| CH3OH(g)浓度(mol?L-1) | c1 | c2 |
| 反应能量变化 | 放出29.4kJ | 吸收akJ |
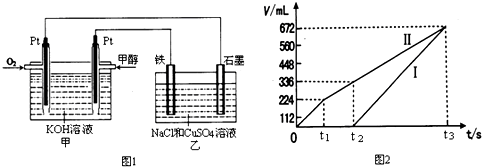
钛在地壳中的含量比铜多61倍,排第十位。钛及其化合物大量应用于航空、造船、电子、化学、医疗器械、电讯器材等各个领域。
⑴ 由钛铁矿(FeTiO3)提取金属钛(海绵钛)的主要工艺过程如下(部分产物省略):

上述熔炼过程发生的反应为吸热反应,该反应能够自发进行的原因是 ▲ ;还原过程必须在1070K的温度下进行,你认为还应该控制的反应条件是 ▲ 。
⑵ 用浓硫酸处理钛铁矿,并向所得溶液中加入铁,此时溶液中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当溶液的pH等于 ▲ 时,Mg(OH)2开始沉淀。
 若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量
若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量
白色沉淀,写出该反应的离子方程式: ▲ 。
⑶ BaTiO3是一种可用来吸收低频波的无机功能材料。工业上,常用
BaCl2、TiCl4、H2O和H2C2O4混合反应生成白色固体A,将该白色
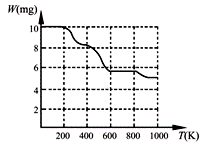
固体加热分解至900K可得BaTiO3,实验测得其热分解过程的质量
-温度关系曲线如右图所示,图中400K、600K和900K时对应的
样品的质量分别为8.38mg、5.68mg和5.19mg。白色固体A的化学式
为 ▲ (填序号)。
a.BaTi2O5 b.BaC2O4·2H2O c.BaTi(C2O4)3 d.BaTiO (C2O4)2·4H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com