
题目列表(包括答案和解析)
|
已知合成氨的反应为:N2(g)+3H2(g) | |
| [ ] | |
A. |
2Q2<Q1<Q |
B. |
2Q2=Q1<Q |
C. |
2Q2=Q1=Q |
D. |
Q1=Q2=Q |
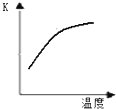 科学家一直致力于“人工固氮”的新方法研究.
科学家一直致力于“人工固氮”的新方法研究.| 4 |
| 27 |
| 4 |
| 27 |
| c(NH3?H2O) |
| c(OH-) |
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
| c(H+) |
| c(OH-) |
| 时间/物质的量 | n(NH3) (mol) | n(O2 ) (mol) | n(NO) (mol) |
| 起始 | 1.600 | 3.200 | 0.000 |
| 第2min | a | 2.700 | 0.4000 |
| 第4min | 0.600 | 1.950 | 1.000 |
| 第6min | 0.600 | 1.950 | 1.000 |
(8分) 关于反应热请回答如下问题:
(1)向1L1mol/L的NaOH溶液中加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应为△H1、△H2、△H3,则三者由小到大顺序为 。
(2) 实验测得,向200mL1mol/L的NaOH溶液中加入稀醋酸恰好反应放出Q kJ的热量,请写出热化学反应方程式:_________________________ 。
(3)已知反应CH3—CH3(g)―→CH2=CH2(g)+H2(g),有关化学键的键能如下。
| 化学键 | C—H | C=C | C—C | H—H |
| 键能/kJ·mol-1 | 414.4 | 615.3 | 347.4 | 435.3 |
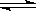 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol| 化学键 | C—H | C=C | C—C | H—H |
| 键能/kJ·mol-1 | 414.4 | 615.3 | 347.4 | 435.3 |
 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com