
题目列表(包括答案和解析)
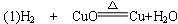
试通过计算回答〔①气体体积按标准状况计,②Ar(Cu)=63.5,Ar(O)=16.0,Ar(H)=1.00〕:
(1)下列H2球较适合用于本实验的是_____________(填选项编号)。
A.500 mL H2球 B.896 mL H2球 C.1500 mL H2球
(2)反应至黑色全部变为红色止,测量H2球的体积变为220 mL,固体质量变为2.700 g,碱石灰增重0.540 g。则:
①参加反应的H2的质量为:______________;
②假设红色物质为单一物质,则红色物质的化学式为_______________________________。
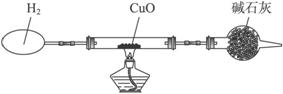
试通过计算回答〔①气体体积按标准状况计,②Ar(Cu)=63.5,Ar(O)=16.0,Ar(H)=1.00〕:
(1)下列氢气球较适合用于本实验的是_______________(填选项编号)。
A.500 mL 氢气球 B.896 mL 氢气球 C.1 500 mL 氢气球
(2)反应至黑色全部变为红色止,测得氢气球的体积变为220 mL,固体质量变为
①参加反应的H2的质量为_______________;
②假设红色物质为单一物质,则红色物质的化学式为_______________。
某课外活动小组设计了如下图所示(夹持装置已略去)的一套装置,用H2和CuO冶炼Cu.准确称取3.180 g CuO放在硬质玻璃管内.已知:CuO-黑色、Cu2O-红色、Cu-红色.
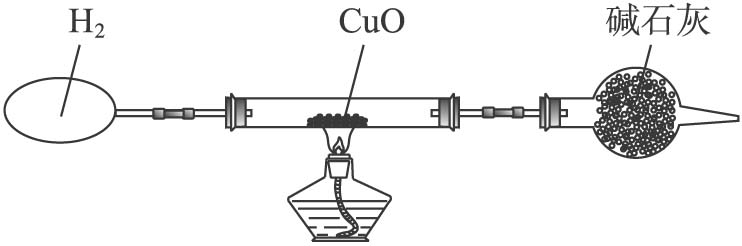
试通过计算回答[①气体体积按标准状况计,②Ar(Cu)=63.5,Ar(O)=16.0,Ar(H)=1.00]:
(1)下列氢气球较适合用于本实验的是________(填选项编号).
A.500 mL氢气球
B.896 mL氢气球
C.1 500 mL氢气球
(2)反应至黑色全部变为红色止,测得氢气球的体积变为220 mL,固体质量变为2.700 g,碱石灰增重0.540 g.则:
①参加反应的H2的质量为________;
②假设红色物质为单一物质,则红色物质的化学式为________.
某课外活动小组设计了如图所示(夹持装置已略去)的一套装置,用H2和CuO冶炼Cu。准确称取3.180 g CuO放在硬质玻璃管内.已知:CuO—黑色、Cu2O—红色、Cu—红色。
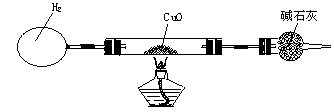
试通过计算回答[①气体体积按标准状况计,②Ar(Cu)=63.5,Ar(O)=16.0,Ar(H)=1.00]:
(1)下列H2球较适合用于本实验的是__________(填选项编号)
A.500 mL H2 球 B.896 mL H2 球 C.1500 mL H2 球
(2)反应至黑色全部变为红色止,测量H2球的体积变为220 mL,固体质量变为2.700 g,碱石灰增重0.540 g。则:
①参加反应的H2的质量为:__________;
②假设红色物质为单一物质,则红色物质的化学式为_______________。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com