
题目列表(包括答案和解析)
 四川盛产井盐,由井盐提取的食盐是日常生活必需品,也是重要的化工原料.
四川盛产井盐,由井盐提取的食盐是日常生活必需品,也是重要的化工原料.2- 4 |
| 加入试剂 |
| 过滤 |
| 适量盐酸 |
| 蒸发、结晶、烘干 |
2- 4 |
| ||
| ||
| ||
ρV1-
|
| ||
ρV1-
|
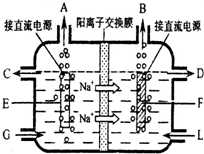
A.阳极:白色阴极:蓝色 B.阳极:蓝色阴极:红色
C.阳极:蓝色阴极:蓝色 D.阳极:蓝色阴极:白色
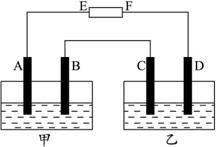
图1-9
(1)电池中E是______________极,F是______________极。
(2)A极上电极反应为______________,B极上电极反应为______________,C极上电极反应为______________,D极上电极反应为______________。
(3)当电路中通过2.408×1022个电子时停止电解,发现B极上析出1.27 g M,则金属M的相对原子质量为______________。
(4)如果再将外接直流电源的正负极交换接入原电路,当通过1 mol电子后,B极的电极反应为______________。

(1)电池中E是___________极,F是___________极。
(2)A极上电极反应为_____________________,B极上电极反应为_____________________,C极上电极反应为_______________________,D极上电极反应为_____________________。
(3)当电路中通过2.408×1022个电子时停止电解,发现B极上析出
(4)如果再将外接直流电源的正负极交换接入原电路,当通过1 mol电子后,B极的电极反应为________________________。
如下图电解装置中,电极A是由金属M制成的,B、C和D都是铂电极,甲中的电解质溶液为MSO4,乙中的电解质为H2SO4.E、F是外接直流电源的两极,电路接通后,电极B上有金属M析出.(已知金属M无变价)

(1)电池中E是_________极,F是_________极.
(2)A极上电极反应为_________,B极上电极反应为_________,C极上电极反应为_________,D极上电极反应为_________.
(3)当电路中通过2.408×1022个电子时停止电解,发现B极上析出1.27 g M,则金属M的相对原子质量为_________.
(4)如果再将外接直流电源的正负极交换接入原电路,当通过1 mol电子后,B极的电极反应为_________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com