
题目列表(包括答案和解析)
下列说法中正确的是( )
| A.0.1 mol?L?1NH4Cl溶液的KW大于0.01mol?L?1NH4Cl溶液的KW |
| B.当镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
C.N2(g)+3H2(g)  2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大 2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大 |
| D.水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应 |
| A.0.1 mol?L?1NH4Cl溶液的KW大于0.01mol?L?1NH4Cl溶液的KW |
| B.当镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
C.N2(g)+3H2(g) 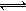 2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大 2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大 |
| D.水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应 |
下列说法不正确的是
A.反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H<0
B.常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小
C.铅蓄电池在放电过程中,正、负极质量都减小
D.温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变
下列说法不正确的是
A.反应C(s)+CO2(g)=2CO(g) △H>0,在任何条件下均不能自发进行
B.铅蓄电池在放电过程中,正、负极质量都减小
C.常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小
D.温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com