
题目列表(包括答案和解析)
某实验小组的同学对该厂生产印刷电路后所得的废液进行了分析:取50.00 mL废液,向其中加入
(1)该厂生产的废液中所含金属离子有________________________。
(2)该厂原来使用的FeCl3溶液的物质的量浓度____________(反应前后溶液的体积变化忽略?不计)。
(3)若向500.00 mL废液中加入足量的稀硝酸,在标准状况下生成NO气体
(4)另取500.00 mL废液,加入一定量铁屑,充分反应后有铜析出,则所得溶液中Fe2+的物质的量范围为________________________________________。
已知Fe3+的氧化性大于Cu2+,据此性质,某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路.用离子方程式表示其化学原理________.
某实验小组的同学对该厂生产印刷电路后所得的废液进行了分析:取50.00 mL废液,向其中加入0.64 g金属铜,金属铜全部溶解;另取50.00 mL废液,向其中加入足量的AgNO3溶液,析出沉淀43.05 g.请回答以下问题:
(1)该厂生产的废液中所含金属离子有________;
(2)该厂原来使用的FeCl3溶液的物质的量浓度________(反应前后溶液的体积变化忽略不计);
(3)若向500.00 mL废液中加入足量的稀硝酸,在标准状况下生成NO气体4.48 L,则原废液中各金属阳离子的物质的量浓度之比为________;
(4)另取500.00 mL废液,加入一定量铁屑,充分反应后有铜析出,则所得溶液中Fe2+的物质的量范围为________.
(16分)已知二元酸H2A在水中存在以下电离:H2A===H++HA-, HA-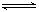 H++A2-,试回答下列问题:
H++A2-,试回答下列问题:
(1)NaHA溶液呈________性,理由是 。
(2)某温度下,向10 mL 0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至中性,此时溶液中以下关系一定正确的是________(填写字母)。
| A.c(Na+)+c(K+)=c(HA-)+c(A2-) | B.水的离子积KW=c 2(OH-) 2(OH-) |
| C.V=10 | D.c(K+)<c(Na+) |
 已知难溶物CaA在水中存在溶解平衡;CaA(s)
已知难溶物CaA在水中存在溶解平衡;CaA(s) 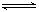 Ca2++A2-;ΔH>0。
Ca2++A2-;ΔH>0。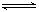 H++A2-,试回答下列问题:
H++A2-,试回答下列问题:| A.c(Na+)+c(K+)=c(HA-)+c(A2-) | B.水的离子积KW=c 2(OH-) 2(OH-) |
| C.V=10 | D.c(K+)<c(Na+) |
 已知难溶物CaA在水中存在溶解平衡;CaA(s)
已知难溶物CaA在水中存在溶解平衡;CaA(s) 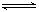 Ca2++A2-;ΔH>0。
Ca2++A2-;ΔH>0。湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com