
题目列表(包括答案和解析)
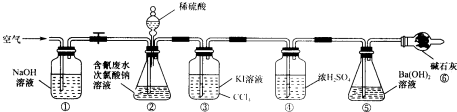
| 实验 | c(H2SO4)mol.L-1 | V(H2SO4)mL | V(NaClO)mL | 含氯废水的体积mL |
| 1 | 100 | 100 | ||
| 2 | 0.0500 | 100 | 100 | |
| 3 | 0.2000 | 100 | 100 |
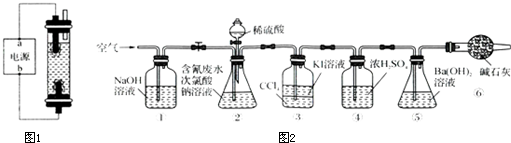


| 实验 | c(H2SO4)mol.L-1 | V(H2S O4)mL | V(NaClO)mL | 含氯废水的体积mL |
| 1 | ______ | 100 | ______ | 100 |
| 2 | 0.0500 | ______ | 100 | 100 |
| 3 | 0.2000 | ______ | 100 | 100 |
某科学实验小组欲用如下图所示的实验装置来验证牺牲阳极的阴极保护法的原理.已知:
3Fe2++2Fe(CN)63-(黄色)
实验步骤如下:
[实验I]向100 mL烧杯中加入约50 mL饱和食盐水后,插入两个玻璃筒(无底).将一根锌棒和一根铁棒用导线与电流计连接后,再分别插入两个玻璃筒中,可以看到电流计指针发生偏转.
(1)电流计指针发生偏转的原因是________.锌棒上发生的反应为________,铁棒上发生的反应为________.
(2)可以证明该实验中无Fe2+产生的现象是________.
[实验II]为了进一步探究金属腐蚀的原理,该小组的同学又做了如下实验:
a.向100 mL烧杯中加入约50 mL饱和食盐水后,插入两个玻璃筒(无底);
b.将一根铜棒与一根铁棒用导线与电流计连接后,再分别插入两个玻璃筒中;
c.1 min后,向插入铁棒的玻璃筒内滴入2~3滴K3[Fe(CN)6]溶液;
d.向插入铜棒的玻璃筒内滴入酚酞溶液.
(3)b步骤中观察到电流计指针偏转但其偏转方向与实验I相反,表明________.
(4)c步骤中观察到的现象是________,表明________.
(5)d步骤中观察到的现象是________,表明________.
(6)通过上述实验可以得出的结论是________.
 铁是人类生产和生活中必不可少的重要金属(如图).
铁是人类生产和生活中必不可少的重要金属(如图).湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com