
题目列表(包括答案和解析)
如图,盛有足量水的水槽里放两个烧杯,小烧杯里放有少量铜片和过量浓硝酸,小烧杯外面倒扣一个大烧杯,请回答:
![]()
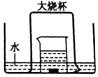 (1)铜与浓硝酸反应的化学方程式:_______________________;
(1)铜与浓硝酸反应的化学方程式:_______________________;
![]() (2)实验中观察到的主要现象是:
(2)实验中观察到的主要现象是:
![]() ①_______________________________ ;
①_______________________________ ;
![]() ②_______________________________ ;
②_______________________________ ;
![]() ③_______________________________ ;
③_______________________________ ;
![]() ④_______________________________ 。
④_______________________________ 。
![]() (3)用该装置做铜与浓硝酸反应实验的优点:______________ ;
(3)用该装置做铜与浓硝酸反应实验的优点:______________ ;
![]() (4)大烧杯内最终所得气体产物的化学式: ;若要验证此气体产物,最简便的方法:_________________________________________ 。
(4)大烧杯内最终所得气体产物的化学式: ;若要验证此气体产物,最简便的方法:_________________________________________ 。

 (1)铜与浓硝酸反应的化学方程式:_______________________;
(1)铜与浓硝酸反应的化学方程式:_______________________; (2)实验中观察到的主要现象是:
(2)实验中观察到的主要现象是: ①_______________________________ ;
①_______________________________ ; ②_______________________________ ;
②_______________________________ ; ③_______________________________ ;
③_______________________________ ; ④_______________________________ 。
④_______________________________ 。 (3)用该装置做铜与浓硝酸反应实验的优点:______________ ;
(3)用该装置做铜与浓硝酸反应实验的优点:______________ ; (4)大烧杯内最终所得气体产物的化学式: ;若要验证此气体产物,最简便的方法:_________________________________________ 。
(4)大烧杯内最终所得气体产物的化学式: ;若要验证此气体产物,最简便的方法:_________________________________________ 。 (1)实验过程中,一定能观察到的现象有:(所需空白数可根据需要增减)
(1)实验过程中,一定能观察到的现象有:(所需空白数可根据需要增减) 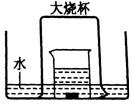 在如下图所示的实验装置中,盛有足量水的水槽里放两个烧杯,小烧杯里放有少量铜片和过量浓硝酸,小烧杯外面倒扣一大烧杯,请回答下列问题:
在如下图所示的实验装置中,盛有足量水的水槽里放两个烧杯,小烧杯里放有少量铜片和过量浓硝酸,小烧杯外面倒扣一大烧杯,请回答下列问题:
(1)实验过程中,观察到的主要现象是:
①铜片表面产生气泡,铜片变小并逐渐消失;;
②小烧杯中溶液的颜色逐渐变成蓝绿色;
③________________________________________________;
④ 大烧杯内液面略有上升,水槽中液面略有下降。
(2)欲使反应现象更明显,应向小烧杯中加入__________。
A、粗铜片 B、纯铜片
(3)用该装置做铜与浓硝酸反应的实验,最突出的优点是:
_________________________________________________________________________。
(4)若要验证最终得到的气体生成物,最简便的方法是:
_________________________________________________________________________。
(5)工业上吸收NO和NO2的混合气体,常使用NaOH溶液(知NO + NO2 +2NaOH==2NaNO2+H2O)。欲使NO和NO2被充分吸收,则NO和NO2的体积应满足_______。
A.V(NO)>V(NO2) B、V(NO)<V(NO2) C、V(NO)≤V(NO2)
 (1)实验过程中,一定能观察到的现象有:(所需空白数可根据需要增减)
(1)实验过程中,一定能观察到的现象有:(所需空白数可根据需要增减)湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com