
题目列表(包括答案和解析)
【解析】A项电荷守恒等式为:c(H+)+c(Na+)=c(OH-)+c(HSO3-)+c(HCO3-)+2c(CO32-) +2c(SO32-),溶液呈中性,c(H+)=c(OH-),导出c(Na+)=c(HSO3-)+c(HCO3-)+2c(CO32-)+2c(SO32-),A项不正确。
B项中的电荷守恒式为:c(Na+)+c(H+)=c(Cl-)+c(CH3COO-)+c(OH-),溶液呈中性,c(H+)=c(OH-),导出c(Na+)=c(Cl-)+c(CH3COO-);根据物料守恒有c(Na+)=c(CH3COOH)+c(CH3COO-),由此二式导出c(Cl-)=c(CH3COOH),综上所述,有c(Na+)>c(Cl-)=c(CH3COOH),B项不对
C项中,NH4+水解呈酸性,CO32-水解呈碱性,它促进NH4+的水解;Fe2+水解呈酸性,它抑制NH4+的水解,所以三种溶液中c(NH4+):③>②>①,C项正确。
D项中,盐类的水解促进水的电离,强酸和弱酸都会抑制水的电离,当c(H+)相同时,对水的电离产生的抑制作用相同,正确的顺序应为①>②=③,D项不对。
【答案】C
【解析】A中c(H2CO3)的系数为2;B中反应后溶液显酸性;D氢离子的物质的量浓度之比为10∶1;A、 B、 D错。由c(Na+)+ c(H+)= c(OH-)+ c(B -),得c(Na+)- c(B -)= c(OH-)-
c(H+),计算就可以了
【答案】C
符合如图所示的热化学方程式是 ( )
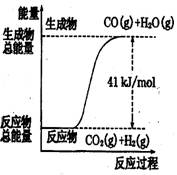
A、CO+H2O=CO2+H2;△H=+41 kJ/mol
B、CO(g)+H2O(g)=CO2(g)+H2(g);;△H= −41 kJ/mol
C、CO2(g)+H2(g)=CO(g)+H2O(g);△H=+41 kJ/mol
D、CO2(g)+H2(g) =CO(g)+H2O(g);△H=−41 kJ/mol
【解析】根据图像可判断反应物的总能量低于生成物的总能量,反应是吸热反应。B、D不正确。在选项A中没有标明物质的状态,是错误的,所以正确的答案是C。
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的3倍 ,下列说法中不正确的是( )
| X | Y |
|
|
| Z | W |
A.四种元素的氢化物中,Y的氢化物沸点最高
B.Z的单质不溶于水,有多种同素异形体
C.阴离子的还原性:X< Y
D. X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐
【解析】考查元素周期表的结构和元素周期律的应用。Y原子的最外层电子数是次外层电子数的3倍,所以Y只能是O,则根据元素在周期表中的位置可知X是N、Z是S、W是Cl。水分子中存在氢键,沸点最高。硫有多种同素异形体,其单质不溶于水。氨气和硝酸反应生成硝酸铵。非金属性是O大于N,所以阴离子的还原性是X>Y,因此正确的答案是C。
下面的排序不正确的是
A.晶体熔点由低到高:CF4<CCl4<CBr4<CCI4
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.熔点由高到低:Na>Mg>Al
D.晶格能由大到小:NaF> NaCl> NaBr>NaI
【解析】A中物质形成的晶体是分子晶体,其熔点和分子间作用力有关,相对分子质量越大,分子间作用力就越大,A正确。在原子晶体中共价键越强,硬度越大。形成共价键的原子半径越小,共价键越强,碳原子比较小于硅原子半径,所以B正确C中物质形成的晶体是金属晶体,金属晶体中金属键越强,熔点越高。而金属键强弱与金属阳离子半径和所带的电荷数有关,阳离子半径越小,电荷数越多,金属键越强,所以熔点由高到低是Na<Mg<Al,C不正确。D中物质全部是离子晶体,形成离子晶体的离子键越强,晶格能越大。形成离子键的离子半径越小,所带电荷数越多,离子键越强,所以D是正确的。答案选C。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com