
题目列表(包括答案和解析)
(NH4)2PtCl6晶体受热分解,生成氮气、氯化氢、氯化铵和金属铂,在此分解反应中,氧化产物与还原产物的物质的量之比是
A.2:3 B.3:2 C.4:3 D.1:3
【解析】根据反应前后的元素的化合价变化可判断,N元素由-3价升高到0,即氮气是氧化产物,每生成1mol氮气转移6mol电子。Pt的化合价由+4价降低到0价,所以Pt是还原产物。根据得失电子守恒可知生成铂的物质的量是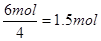 ,所以氧化产物和还原产物的物质的量之比是2:3,选项A正确。答案选A。
,所以氧化产物和还原产物的物质的量之比是2:3,选项A正确。答案选A。
构成下列四种物质的微粒间,既存在离子键又存在共价键的是( )
A.KOH B.K2S C.MgCl2 D.SO3
【解析】考查化学键的判断。一般情况下活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键,所以选项A、B、C、D中含有的化学键分别为离子键和极性键、离子键、离子键、极性键。因此答案是A。
与氢氧根离子具有相同的质子数和电子数的微粒是( )
A.CH4 B.NH4+ C.NH2- D.Cl-
【解析】OH-含有的质子数和电子数分别为9和10,选项A、B、C、D中含有的质子数和电子数分别为10和10、11和10、9和10、17和18。所以答案是C。
(NH4)2PtCl6晶体受热分解,生成氮气、氯化氢、氯化铵和金属铂,在此分解反应中,氧化产物与还原产物的物质的量之比是
A.2:3 B.3:2 C.4:3 D.1:3
【解析】根据反应前后的元素的化合价变化可判断,N元素由-3价升高到0,即氮气是氧化产物,每生成1mol氮气转移6mol电子。Pt的化合价由+4价降低到0价,所以Pt是还原产物。根据得失电子守恒可知生成铂的物质的量是![]() ,所以氧化产物和还原产物的物质的量之比是2:3,选项A正确。答案选A。
,所以氧化产物和还原产物的物质的量之比是2:3,选项A正确。答案选A。
30 mL一定浓度的硝酸溶液与5.44g铜片反应,当铜片全部反应完毕后,共收集到
气体2.24 L(标准状况下),则该硝酸溶液的物质的量浓度至少为( )
A.9 mol/L B.8 mol/L C.5 mol/L D.10 mol/L
【解析】5.44g铜是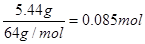 ,则反应后生成的硝酸铜也是0.085mol,即没有被还原的硝酸是0.085mol×2=0.17mol。硝酸的还原产物是NO和NO2的混合物,因此被还原的硝酸是
,则反应后生成的硝酸铜也是0.085mol,即没有被还原的硝酸是0.085mol×2=0.17mol。硝酸的还原产物是NO和NO2的混合物,因此被还原的硝酸是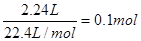 ,所以原硝酸的物质的量至少是0.27mol,其浓度至少为
,所以原硝酸的物质的量至少是0.27mol,其浓度至少为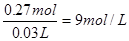 。即选项A是正确的。答案是A。
。即选项A是正确的。答案是A。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com