铁及其化合物在国民经济的发展中起着重要作用.
(1)已知:4Fe(s)+3O
2(g)=2Fe
2O
3(s)△H=-1641.0kJ?mol
-1C(石墨)+1/2O
2(g)=CO(g)△H=-110.5kJ?mol
-1则Fe
2O
3(s)+3C(石墨)=2Fe(s)+3CO(g)的△H=
+489.0kJ/mol
+489.0kJ/mol
kJ?mol
-1.
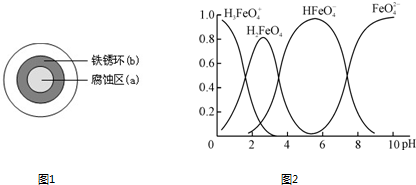
(2)铁在潮湿的空气中易发生电化学腐蚀.某同学将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图1所示.液滴边缘是
正极
正极
区(填“正极”或“负极”),其电极反应式为
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.
(3)铁钛合金是一种常用的不锈钢材料,某同学在探究该合金的性质时,往含有TiO
2+、Fe
3+溶液中加入铁屑至溶液显紫色,该过程中发生的反应有:
①2TiO
2+(无色)+Fe+4H
+=2Ti
3+(紫色)+Fe
2++2H
2O
②Ti
3+(紫色)+Fe
3++H
2O=TiO
2+(无色)+Fe
2++2H
+③
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.
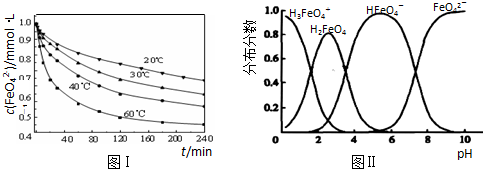
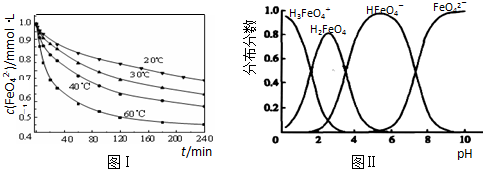
(4)①高铁酸钾(K
2FeO
4)是一种优良的水处理剂.
在水溶液中的存在形态如图2所示,纵坐标表示各存在形态的分数分布.
下列说法不正确的是
AB
AB
.(填字母)
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFe
的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:HFe
+OH
-═Fe
+H
2O
②K
2FeO
4溶于水会放出一种无色无味气体,其杀菌消毒、吸附水中的悬浮杂质的原理可用离子方程式表示为
4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑
4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2↑
.
(5)向一定量的Fe、FeO、Fe
3O
4的混合物中加入100mL 1mol?L
-1的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)气体,加入KSCN溶液不显红色.若用足量的CO在高温下还原相同质量的此混合物,可得铁
2.8
2.8
g.