
题目列表(包括答案和解析)
(7分)某工业纯碱中含有少量NaCl和NaOH。学生课外活动小组为测定其中Na2CO3的质量分数,采样进行分析。通过集体讨论,选择下列适当装置连接,对设计方案不断完善,成功地完成了测定实验。
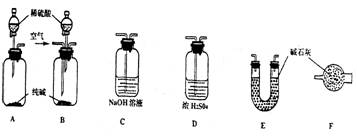
下面是甲、乙、丙、丁、戊五位同学有关设计实验装置的讨论发言。请在空白处填写他们的发言内容:
甲: 将装置A和E连接即可。因为Na2CO3与稀硫酸反应生成的CO2被E中的碱石灰吸收,通过分别测量反应前和反应后E的总质量,可求出Na2CO3的质量分数。
乙: 还应在A和E之间连接装置_____(填序号),其目的是: _________________________
丙:应该用B装置取代A。从B装置的导管口处缓缓鼓入空气,其目的是:
_______________________________________________________________
丁: 由于空气中含有CO2,若直接向B装置鼓入空气会导致实验测定结果__________(填“偏高”、“偏低”或“无影响”)。因此,应将鼓入的空气先通过装置________。
戊: E装置后还应连接装置F,其作用是___________________________________________
学生课外活动小组测定的数据如下:

计算该工业纯碱中Na2CO3的质量分数为: ___________
(7分)某工业纯碱中含有少量NaCl和NaOH。学生课外活动小组为测定其中Na2CO3的质量分数,采样进行分析。通过集体讨论,选择下列适当装置连接,对设计方案不断完善,成功地完成了测定实验。
下面是甲、乙、丙、丁、戊五位同学有关设计实验装置的讨论发言。请在空白处填写他们的发言内容:
甲: 将装置A和E连接即可。因为Na2CO3与稀硫酸反应生成的CO2被E中的碱石灰吸收,通过分别测量反应前和反应后E的总质量,可求出Na2CO3的质量分数。
乙: 还应在A和E之间连接装置_____(填序号),其目的是: _________________________
丙:应该用B装置取代A。从B装置的导管口处缓缓鼓入空气,其目的是:
_______________________________________________________________
丁: 由于空气中含有CO2,若直接向B装置鼓入空气会导致实验测定结果__________(填“偏高”、“偏低”或“无影响”)。因此,应将鼓入的空气先通过装置________。
戊: E装置后还应连接装置F,其作用是___________________________________________
学生课外活动小组测定的数据如下:
计算该工业纯碱中Na2CO3的质量分数为: ___________
某工业纯碱中含有少量NaCl和NaOH.学生课外活动小组为测定其中Na2CO3的质量分数,采样进行分析.通过集体讨论,选择下列适当装置连接,对设计方案不断完善,成功地完成了测定实验.
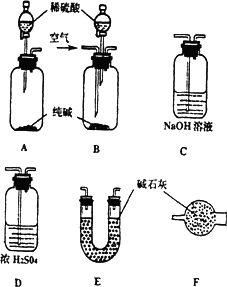
下面是甲、乙、丙、丁、戊五位同学有关设计实验装置的讨论发言.请在空白处填写他们的发言内容:
甲:将装置A和E连接即可.因为Na2CO3与稀硫酸反应生成的CO2被E中的碱石灰吸收,通过分别测量反应前和反应后E的总质量,可求出Na2CO3的质量分数.
乙:还应在A和E之间连接装置________(填序号),其目的是:________
丙:应该用B装置取代A.从B装置的导管口处缓缓鼓入空气,其目的是:________
丁:由于空气中含有CO2,若直接向B装置鼓入空气会导致实验测定结果________(填“偏高”、“偏低”或“无影响”).因此,应将鼓入的空气先通过装置________.
戊:E装置后还应连接装置F,其作用是________
学生课外活动小组测定的数据如下:
![]()
计算该工业纯碱中Na2CO3的质量分数为:________
[相对原子质量:C-12 O-16 Na-23]
(7分)某工业纯碱中含有少量NaCl和NaOH。学生课外活动小组为测定其中Na2CO3的质量分数,采样进行分析。通过集体讨论,选择下列适当装置连接,对设计方案不断完善,成功地完成了测定实验。
下面是甲、乙、丙、丁、戊五位同学有关设计实验装置的讨论发言。请在空白处填写他们的发言内容:
甲: 将装置A和E连接即可。因为Na2CO3与稀硫酸反应生成的CO2被E中的碱石灰吸收,通过分别测量反应前和反应后E的总质量,可求出Na2CO3的质量分数。
乙: 还应在A和E之间连接装置_____(填序号),其目的是: _________________________
丙:应该用B装置取代A。从B装置的导管口处缓缓鼓入空气,其目的是:
_______________________________________________________________
丁: 由于空气中含有CO2,若直接向B装置鼓入空气会导致实验测定结果__________(填“偏高”、“偏低”或“无影响”)。因此,应将鼓入的空气先通过装置________。
戊: E装置后还应连接装置F,其作用是___________________________________________
学生课外活动小组测定的数据如下:
计算该工业纯碱中Na2CO3的质量分数为: ___________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com