
题目列表(包括答案和解析)
下列事实,不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+ H2O HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
B.对CO(g) + NO2 (g) CO2(g)+ NO(g) 平衡体系增大压强可使颜色变深
C.升高温度能够增大硝酸钾在水中的溶解度
D.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施
下列事实,不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+ H2O HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
B.对CO(g) + NO2 (g) CO2(g)+ NO(g) 平衡体系增大压强可使颜色变深
C.升高温度能够增大硝酸钾在水中的溶解度
D.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施
下列事实,不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+ H2O HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
B.对CO(g) + NO2 (g) CO2(g)+ NO(g) 平衡体系增大压强可使颜色变深
C.升高温度能够增大硝酸钾在水中的溶解度
D.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施
下列事实,不能用勒夏特列原理解释的是
A.新制的氯水在光照下颜色变浅
B.H2、I2、HI平衡混合气加压后颜色变深
C.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施
D.实验室用排饱和食盐水而不用排水法收集氯气
下列事实,不能用勒夏特列原理解释的是
A.在溴水中存在如下平衡:Br2+H2O
 HBr+HBrO 当加入NaOH溶液后颜色变浅
HBr+HBrO 当加入NaOH溶液后颜色变浅
B.对2HI H2+I2(g)平衡体系增加压强使颜色变深
H2+I2(g)平衡体系增加压强使颜色变深
C.反应CO+NO2 CO2+NO ΔH<0 升高温度使平衡向逆方向移动
CO2+NO ΔH<0 升高温度使平衡向逆方向移动
D.合成氨反应: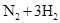

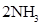 ,ΔH<0 为使氨的产率提高,理论上应采取低温高压的措施
,ΔH<0 为使氨的产率提高,理论上应采取低温高压的措施
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com