
题目列表(包括答案和解析)

下列有关说法正确的是( )
A.碘化亚铁溶液中通入少量氯气的离子方程式为:2Fe2++ Cl2= 2Cl- +2Fe3+
B.对于平衡体系mA(g)+nB(g)![]() pC(g)+qD(g), 若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.45倍,则m+n>p+q
pC(g)+qD(g), 若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.45倍,则m+n>p+q
C.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动,但难溶物的溶度积常数不一定改变
D.在强碱性溶液中,ClO-、Na+、S2-、Cl-可以大量共存
|
对于可逆反应mA(g)+nB(s)
| |
A. |
降温,化学平衡向正反应方向移动 |
B. |
使用催化剂可使w(D)有所增加 |
C. |
化学方程式中气体的化学计量数m<p+q |
D. |
B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动 |
对于mA(g) + nB(g) 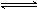 pC(g) + qD(g) 的平衡体系,当升高温度时,体系的平均相对摩尔质量从26变为29,则下列说法正确的是
pC(g) + qD(g) 的平衡体系,当升高温度时,体系的平均相对摩尔质量从26变为29,则下列说法正确的是
A. m+n>p+q,正反应是放热反应 B. m+n>p+q,正反应是吸热反应
C. m+n<p+q,逆反应是放热反应 D. m+n<p+q,正反应是吸热反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com