
题目列表(包括答案和解析)
| A、金属钠的化学性质很活泼,在自然界里不能以游离态存在 | B、金属镁和金属铝容易被空气氧化,所以在空气中必须进行密封保存 | C、金属铁可以和稀硫酸反应放出氢气,但冷的浓硫酸能用铁罐储存运输 | D、金属单质在化学反应中均作还原剂,不能作氧化剂 |
①②③④⑤五种元素,在元素周期表中的位置如图所示。回答下列问题: 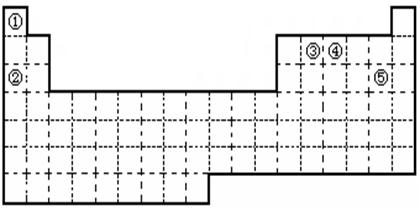
(1)①②③④⑤五种元素中,金属性最强的元素是 (写元素名称), 该元素的单质在空气中燃烧的化学方程式为 。
(2)元素②的最高价氧化物对应的水化物属于 化合物,(填“共价”或“离子” ),其电子式为 , 试比较②和③原子半径的大小
② ③(填“﹥” 或“﹤” )
(3)画出元素④的原子结构示意图 ,该元素的最高价氧化物的
水化物能与Cu发生反应,反应中作氧化剂的是(写化学式) 。
(4)写出元素⑤在周期表中的位置 ,以海水中含量最大的物质为原料可以生产⑤的单质,同时还可以得到另外两种重要的工业原料,该反应的化学方程式为 。
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外L层电子数是M层电子数的4倍。
①甲、乙元素分别为 、 (写元素名称)
②写出②的最高价氧化物对应的水化物与甲的最高价氧化物反应的离子方程式
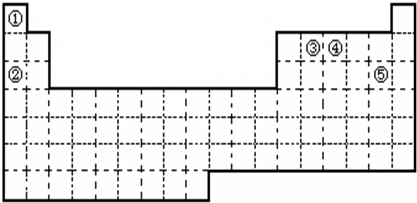
①②③④⑤五种元素,在元素周期表中的位置如图所示。回答下列问题:

(1)①②③④⑤五种元素中,金属性最强的元素是 (写元素名称), 该元素的单质在空气中燃烧的化学方程式为 。
(2)元素②的最高价氧化物对应的水化物属于 化合物,(填“共价”或“离子” ),其电子式为 , 试比较②和③原子半径的大小
② ③(填“﹥” 或“﹤” )
(3)画出元素④的原子结构示意图 ,该元素的最高价氧化物的
水化物能与Cu发生反应,反应中作氧化剂的是(写化学式) 。
(4)写出元素⑤在周期表中的位置 ,以海水中含量最大的物质为原料可以生产⑤的单质,同时还可以得到另外两种重要的工业原料,该反应的化学方程式为 。
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外L层电子数是M层电子数的4倍。
①甲、乙元素分别为 、 (写元素名称)
②写出②的最高价氧化物对应的水化物与甲的最高价氧化物反应的离子方程式

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com