已知乙醇可以和氯化钙反应,生成微溶于水的CaCl
2?6C
2H
5OH.有关试剂的部分数据如下:
| 物 质 |
熔点(℃) |
沸点(℃) |
密度(g/cm3) |
| 乙 醇 |
-117.0 |
78.0 |
0.79 |
| 乙 酸 |
16.6 |
117.9 |
1.05 |
| 乙酸乙酯 |
-83.6 |
77.5 |
0.90 |
| 浓硫酸(98%) |
- |
338.0 |
1.84 |
学生在实验室制取乙酸乙酯的主要步骤如下:
①在30mL的大试管A中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合溶液.
②按如图1所示连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10分钟
③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置,等待分层.
④分离出乙酸乙酯层并洗涤、干燥.
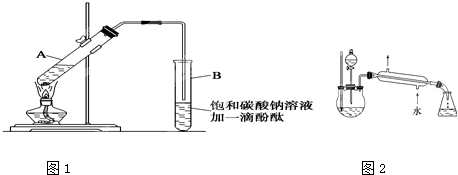
请根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为:
在一个30mL大试管中注入4mL乙醇,再分别缓缓加入4mL乙酸、1mL浓硫酸(乙酸和浓硫酸的加入顺序可互换),边加边振荡试管使之混合均匀(药品总用量不能超过10mL)
在一个30mL大试管中注入4mL乙醇,再分别缓缓加入4mL乙酸、1mL浓硫酸(乙酸和浓硫酸的加入顺序可互换),边加边振荡试管使之混合均匀(药品总用量不能超过10mL)
,写出制取乙酸乙酯的化学方程式:
CH
3COOH+CH
3CH
2OH

CH
3COOCH
2CH
3+H
2O
CH
3COOH+CH
3CH
2OH

CH
3COOCH
2CH
3+H
2O
.
(2)上述实验中饱和碳酸钠溶液的作用是:
BC
BC
(填字母).
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于其分层析出
D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要理由是:
反应物中乙醇、乙酸的沸点较低,若用大火加热,大量反应物随产物蒸发而损失原料,温度过高还可能发生其他副反应
反应物中乙醇、乙酸的沸点较低,若用大火加热,大量反应物随产物蒸发而损失原料,温度过高还可能发生其他副反应
.
(4)指出步骤③所观察到的现象:
在浅红色碳酸钠溶液层上方有无色液体出现,闻到香味,振荡后碳酸钠溶液层红色变浅
在浅红色碳酸钠溶液层上方有无色液体出现,闻到香味,振荡后碳酸钠溶液层红色变浅
;分离出乙酸乙酯层后,一般用饱和食盐水和饱和氯化钙溶液洗涤,可通过洗涤除去
碳酸钠、乙醇
碳酸钠、乙醇
(填名称)杂质;为了干燥乙酸乙酯,可选用的干燥剂为
B
B
(填字母).
A.P
2O
5 B.无水Na
2SO
4 C.碱石灰 D.NaOH固体
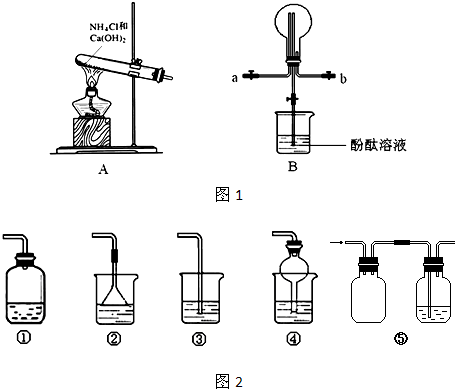
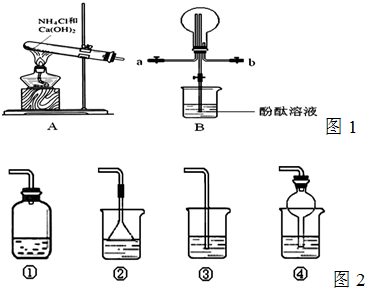
(5)某化学课外小组设计了如图2所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),试分析与上图的装置相比,此装置的主要优点.

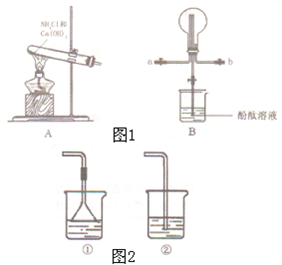 某化学实验小组同学利用如图1装置制备氨气,并探究氨气的性质(部分仪器已略去).
某化学实验小组同学利用如图1装置制备氨气,并探究氨气的性质(部分仪器已略去). 乙:
乙: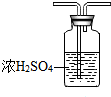 .
.

 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O