
题目列表(包括答案和解析)
[化学——选修物质结构与性质](15分)
在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们的原子最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高。
(1)B元素在周期表中的位置 ;(2分)
D元素基态原子电子排布式为_____________________________。(2分)
(2)E的气态氢化物在同族元素中沸点最高的原因是:
。(2分)
(3)A、C两元素第一电离能 > 。(填元素符号)(2分)
(4)B元素能形成多种配合物。元素之间形成配合物的条件是:一方是能够提供孤对电子的原子,另一方是 的原子。(2分)
(5)A元素可与氢元素形成离子化合物,电子式为_______________;(2分)这种离子化合物可与水反应,化学方程式为________________________________。(3分)
[化学——选修物质结构与性质](15分)
在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们的原子最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高。
(1)B元素在周期表中的位置 ;(2分)
D元素基态原子电子排布式为_____________________________。(2分)
(2)E的气态氢化物在同族元素中沸点最高的原因是:
。(2分)
(3)A、C两元素第一电离能 > 。(填元素符号)(2分)
(4)B元素能形成多种配合物。元素之间形成配合物的条件是:一方是能够提供孤对电子的原子,另一方是 的原子。(2分)
(5)A元素可与氢元素形成离子化合物,电子式为_______________;(2分)这种离子化合物可与水反应,化学方程式为________________________________。(3分)
[化学——选修物质结构与性质](15分)
在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们的原子最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高。
(1)B元素在周期表中的位置 ;(2分)
D元素基态原子电子排布式为_____________________________。(2分)
(2)E的气态氢化物在同族元素中沸点最高的原因是:
。(2分)
(3)A、C两元素第一电离能 > 。(填元素符号)(2分)
(4)B元素能形成多种配合物。元素之间形成配合物的条件是:一方是能够提供孤对电子的原子,另一方是 的原子。(2分)
(5)A元素可与氢元素形成离子化合物,电子式为_______________;(2分)这种离子化合物可与水反应,化学方程式为________________________________。(3分)
[化学——选修物质结构与性质]
在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们的原子最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高。
(1)B元素在周期表中的位置 ;
D元素基态原子电子排布式为_____________________________。
(2)E的气态氢化物在同族元素中沸点最高的原因是:
。
(3)A、C两元素第一电离能 > 。(填元素符号)
(4)B元素能形成多种配合物。元素之间形成配合物的条件是:一方是能够提供孤对电子的原子,另一方是 的原子。
(5)A元素可与氢元素形成离子化合物,电子式为_______________;这种离子化合物可与水反应,化学方程式为________________________________。
[化学——选修物质结构与性质]
A、B、C、D为1~36号元素。A元素的原子价电子排带为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的p亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
(1)当n=2时,AB2属于_____分子(填“极性”或“非极性”),分子中有____个σ键,____个π键。
(2)当n=3时,A与B形成的晶体属于_____晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是___(用元素符号表示)。
(4)已知某红紫色配合物的组成为CoCl3·5NH3·H2O。该配合物中的中心离子钴离子在基态的核外电子排布式为____,作为配位体之一的NH3分子的空间构型为_____。
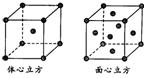
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为_____。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com