
题目列表(包括答案和解析)
工业纯碱中常含有少量NaCl杂质,可用下列装置测定纯碱中碳酸钠的质量分数。如图所示,从D处鼓入空气,A试管盛有NaOH溶液,E是盛有稀硫酸的分液漏斗,B广口瓶中放的是含有NaCl杂质的Na2CO3固体,C为盛有浓硫酸的试管,F、G均为盛有碱石灰的干燥管。
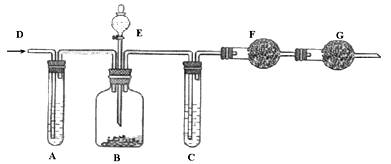
实验操作如下: ①检查装置的气密性;②在干燥管F内填满颗粒状碱石灰,其总质量为m1 g;③称取一定量的纯碱样品m2 g,并放入广口瓶中;④从分液漏斗中缓慢的滴入稀硫酸,至不再产生气体为止;⑤从D处缓慢鼓入空气数分钟,然后再称量干燥管F,其总
质量为m3 g。回答下列问题:
(1)鼓入空气的目的是_____________________________________________。
(2)装置G的作用是_______________________________________________。
(3)装置A的作用是_______________________________________________。
(4)装置C的作用是_______________________________________________。
(5)样品中碳酸钠的质量分数计算式为_______________________________。
(6)如撤去装置A,则将导致实验结果___。(填“偏大”、“偏小”或“不变”)
(7)如撤去装置C,则将导致实验结果______。(填“偏大”、“偏小”或“不变”)
(8)上述实验操作中的④和⑤,都要求实验缓慢进行。如果这两步操作太快,则将导致实验结果__________________。(填“偏大”、“偏小”或“不变”)
工业纯碱中常含有少量NaCl杂质,可用下列装置测定纯碱中碳酸钠的质量分数。如图所示,从D处鼓入空气,A试管盛有NaOH溶液,E是盛有稀硫酸的分液漏斗,B广口瓶中放的是含有NaCl杂质的Na2CO3固体,C为盛有浓硫酸的试管,F、G均为盛有碱石灰的干燥管。

实验操作如下: ①检查装置的气密性;②在干燥管F内填满颗粒状碱石灰,其总质量为m1 g;③称取一定量的纯碱样品m2 g,并放入广口瓶中;④从分液漏斗中缓慢的滴入稀硫酸,至不再产生气体为止;⑤从D处缓慢鼓入空气数分钟,然后再称量干燥管F,其总质量为m3 g。回答下列问题:
(1) 鼓入空气的目的是_____________________________________________。
(2) 装置G的作用是_______________________________________________。
(3)装置A的作用是_______________________________________________。
(4)样品中碳酸钠的质量分数计算式为_______________________________。
(5)如撤去装置A,则将导致实验结果____。(填“偏大”、“偏小”或“不变”)
工业纯碱中常含有少量NaCl杂质,可用下列装置测定纯碱中碳酸钠的质量分数.如图所示,从D处鼓入空气,A试管盛有NaOH溶液,E是盛有稀硫酸的分液漏斗,B广口瓶中放的是含有NaCl杂质的Na2CO3固体,C为盛有浓硫酸的试管,F、G均为盛有碱石灰的干燥管.
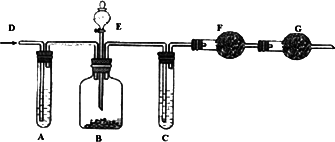
实验操作如下:①检查装置的气密性;②在干燥管F内填满颗粒状碱石灰,其总质量为m1 g;③称取一定量的纯碱样品m2 g,并放入广口瓶中;④从分液漏斗中缓慢的滴入稀硫酸,至不再产生气体为止;⑤从D处缓慢鼓入空气数分钟,然后再称量干燥管F,其总质量为m3 g.回答下列问题:
(1)鼓入空气的目的是________.
(2)装置G的作用是________.
(3)装置A的作用是________.
(4)装置C的作用是________.
(5)样品中碳酸钠的质量分数计算式为________.
(6)如撤去装置A,则将导致实验结果________.(填“偏大”、“偏小”或“不变”)
(7)如撤去装置C,则将导致实验结果________.(填“偏大”、“偏小”或“不变”)
(8)上述实验操作中的④和⑤,都要求实验缓慢进行.如果这两步操作太快,则将导致实验结果________.(填“偏大”、“偏小”或“不变”)
工业纯碱中常含有少量NaCl的杂质,可用下列装置测定纯碱中碳酸钠的质量分数.如图所示,D处鼓入空气,A试管盛有NaOH溶液,F是盛有稀硫酸的分液漏斗,B广口瓶中放的是含有NaCl的Na2CO3固体,C为盛有浓硫酸的试管,E为盛有碱石灰(NaOH和CaO的混合物)的干燥管.
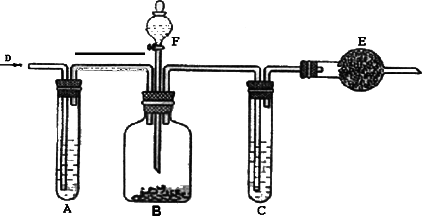
实验操作如下:
①检查装置的气密性.
②在干燥管内填满颗粒状碱石灰,称总重为W1g.
③称取一定量纯碱W2g,并放在广口瓶内.
④缓缓地加入稀硫酸到不产生气体为止.
⑤缓缓鼓入空气约5分钟后,再称干燥管总重为W3g.
试回答下列问题:
(1)鼓入空气的目的和装置E的作用分别是什么?________;________.
(2)装置A的作用是_____________________.
(3)装置C的作用是_____________________.
(4)碳酸钠质量分数计算式为_____________.
(5)如撤去A则测定结果将________.(填“偏大”或“偏小”或“不影响”)
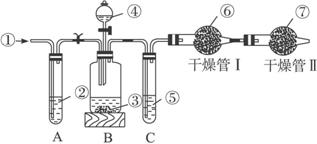
实验步骤:
①检验装置的气密性;
②准确称量盛有碱石灰的干燥管Ⅰ的质量(设为m
③准确称量一定量的纯碱的质量(设为m
④从分液漏斗中缓缓滴入稀H2SO4,至不再产生气体为止;
⑤缓缓鼓入空气数分钟,然后称量干燥管Ⅰ的总质量(设为m
根据以上实验,回答下列问题:
(1)鼓入空气的目的是____________________________________________________。
(2)装置A中液体应用____________,其作用是______________________,如撤去装置A,直接向装置B中缓缓鼓入空气,测定结果将_____________(填“偏大”“偏小”或“不变”)。
(3)装置C的作用是__________________________________________________,如果撤去C,则会导致实验结果______________(填“偏大”“偏小”或“不变”)
(4)干燥管Ⅱ的作用是___________________________________________________。
(5)上述实验的操作④和⑤,都要求缓缓进行,其理由是______________,如果这两步操作太快,则会导致实验测定结果______________(填“偏大”“偏小”或“不变”)。
(6)根据实验,纯碱中Na2CO3的质量分数的计算式为______________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com