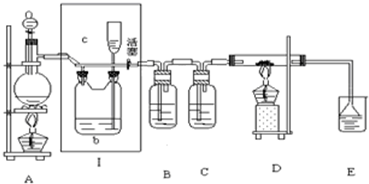
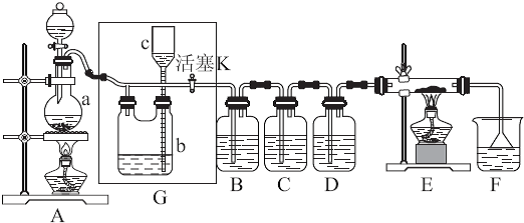
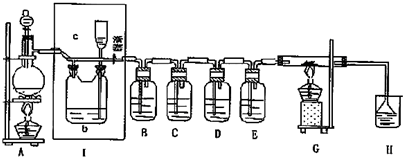
如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为:B(碘化钾淀粉溶液),C(水),E(紫色石蕊试液).
(1)A是氯气发生装置,蒸馏烧瓶中盛放MnO
2固体,分液漏斗中盛放浓盐酸,实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃D处酒精灯.请回答以下问题:
①怎样证明氯气已经充满了整个装置
观察当整个装置内充满黄绿色气体时,说明氯气已充满整个装置
观察当整个装置内充满黄绿色气体时,说明氯气已充满整个装置
;
②B中的实验现象是
溶液变蓝
溶液变蓝
.
(2)在D装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,一种产物能使E处紫色石蕊试液变红,另一产物能使澄清石灰水变浑浊,根据信息写出D中反应的化学方程式
.
(3)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是
生成的HCl使紫色石蕊试液变红色,剩余的氯气又与水作用生成次氯酸,又起漂白作用,使红色褪去
生成的HCl使紫色石蕊试液变红色,剩余的氯气又与水作用生成次氯酸,又起漂白作用,使红色褪去
.
(4)D处反应完毕后关闭分液漏斗旋塞,移去酒精灯,但由于余热的作用,A处仍有氯气产生,此时应该怎样操作
关闭Ⅰ处活塞
关闭Ⅰ处活塞
;装置Ⅰ中的现象是
Ⅰ处b瓶内液面下降,c中液面上升
Ⅰ处b瓶内液面下降,c中液面上升
.
(5)若将C中的水换成氢氧化钠溶液,溶液中不但有NaClO还有NaClO
3,其物质的量比为2:1,则参加反应的氧化剂和还原剂的物质的量比为:
7:3
7:3
.