
题目列表(包括答案和解析)
下列说法正确的是
A、强氧化物与强还原剂一定能发生氧化还原反应
B、弱电解质被稀释时,离子浓度一定减小
C、1 mol某气体的体积是22.4 L,该气体所处的状态一定是标准状态
D、有单质参加或生成的化学反应不一定是氧化还原反应
下列说法正确的是:
[ ]
A.金属钠又叫苛性钠.
B
.钠原子有强还原性,钠离子有强氧化性.C
.钠与硫酸铜溶液反应,能置换出铜,没有其它单质生成.D
.钠是一种很强的还原剂, 可把钛、钽、铌、锆等金属从它们熔融的氯化物中还原出来.A、B、C、D、E为五种常见的短周期元素,常温下,A、B可形成B2A2和B2A两种液态化合物,B与D可组成分子X,X水溶液呈碱性,C元素的焰色反应呈黄色,E与C同周期,且E的简单离子半径是同周期元素形成的简单离子中半径最小的。试回答:
(1)D元素在周期表中的位置为 。
(2)B2 A和X的分子结合质子 的能力不同,只用一个离子方程式就能证明,写出该离子反应方程式 。
(3)A、D、E三种元素形成的盐(化学式A9D3E)的水溶液呈酸性,用离子方程式解释其原因 ;
(4)W、Q是由A、B、C、D四种元素中任意三种组成的不同类型的强电解质,常温下0.1mol·L—1W的水溶液的pH为13,Q的水溶液呈酸性且能和W反应放出气体,物质的量浓度相同的 W、Q溶液中水的电离程度是前者小于后者。则:W为 ,Q为 (填化学式)。
(5)B和E形成的化合物E2B6常在有机合成中作强还原剂,甚至可将二氧化碳重新还原成甲烷,写出该反应方程式 。
(6)已知工业合成X的反应方程式:D2
(g)+3B2 (g)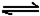 2X(g);△H
=-92.4 kJ·mol-1 ,在适当的催化剂和恒温恒压条件下反应,下列说法正确的有 。
2X(g);△H
=-92.4 kJ·mol-1 ,在适当的催化剂和恒温恒压条件下反应,下列说法正确的有 。
A.达到化学平衡时,正逆反应速率相等
B.反应过程中不断分离出X,使平衡常数K减小,平衡正向移动有利于合成X
C.达到平衡后,升高温度,平衡常数K增大,B2的转化率降低
D.达到化学平衡的过程中,气体平均相对分子质量减小
A、B、C、D、E为原子序数依次增大的短周期元素。已知A的一种单质是自然界中最硬的物质,B与D同主族,C与E同主族,B的一种单质能用于自来水消毒,C在元素周期表中的非金属性最强。则下列说法正确的是
A. C的最高价氧化物对应的水化物的酸性最强
B. 最简单气态氢化物的稳定性E>D>B
C.A与B形成的化合物在反应中只能作还原剂
D.A分别与其他四种元素形成的化合物一定是共价化台物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com