
题目列表(包括答案和解析)
| ||
| ||

| ||
| ||
 Al(OH)3+3H+
Al(OH)3+3H+ Al(OH)3+3H+
Al(OH)3+3H+
| ||
| ||
(16分)A、B、C、D、E是中学常见的五种物质,其转化关系如下图示。反应I、II均在水溶液中进行,其中某些物质可能已略去。已知D是单质,C、E是化合物。
(1)若A是单质,其水溶液具有漂白性,D在常温下为固态,且A、D均可使湿润的淀粉碘化钾试纸变蓝。E是一种可溶性强碱,其焰色反应为黄色。
①E的电子式为 ;C固态时的晶体类型为 ;
②写出反应II的离子方程式 ;
③在E的环境中,A与B还可以发生另外一个反应,每1mol B完全反应转移6 mol电子,写出反应的化学方程式 。
(2)若B是单质,工业上用电解氧化物的方法获得B。B元素原子的电子层数等于其最外层电子数。D是无色无味的气体,E是B的最高价氧化物的水化物。
①若C溶液显酸性,其原因用离子方程式表示为 ;
②若C溶液显碱性,则反应II的离子方程式为 。
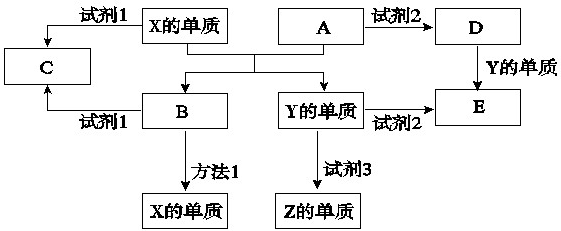
(10分)A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
回答下列问题:
(1)X的单质与A反应的化学方程式是 。
(2)若C溶液显碱性,则试剂1是 液溶(写化学式):若C溶液显酸性,则显酸性的原因是(用离子方程式表示) 。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是 ;
②写出D→E反应的离子方程式 ;
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠(NaNO2)为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是(不必配平): [来源: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com