(化学--选修化学与技术)
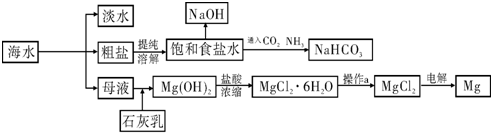
海水中溶解了大量的气体物质和各种盐类.人类在陆地上发现的100多种元素,在海水中可以找到80多种.海洋是一个远未完全开发的巨大化学资源宝库,海洋资源的综合利用具有非常广阔的前景.回答下列问题:
(1)蒸馏法是人类最早使用的淡化海水的方法,技术和工艺比较完备,但由于使用大量燃煤,因此能耗多、排污量大.为克服蒸馏法海水淡化的缺陷,请你对蒸馏法淡化海水的工艺提出一条改进建议
充分利用潮汐能、风能、太阳能等海边富有的洁净能源
充分利用潮汐能、风能、太阳能等海边富有的洁净能源
.
(2)使用离子交换树脂与水中的离子进行交换也是常用的水处理技术.聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式
CH2=CHCOONa
CH2=CHCOONa
.
(3)空气吹出法是目前从海水中提取溴的常用方法,流程如下(苦卤:海水蒸发结晶分离出食盐后的母液):
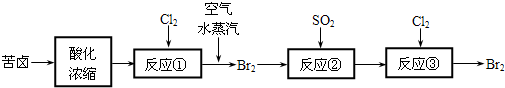
①反应②的离子方程式为
SO2+Br2+2H2O=4H++2Br-+SO42-
SO2+Br2+2H2O=4H++2Br-+SO42-
; ②从反应③后的四氯化碳溶液中分离出单质溴的方法是
蒸馏
蒸馏
.
(4)苦卤中含有NaCl、MgCl
2、KCl、MgSO
4.用简要的文字说明如何测定苦卤中MgCl
2的含量
先用足量BaCl2溶液沉淀硫酸根离子,求出硫酸根离子的总量,并求出MgSO4的量,然后用足量NaOH溶液沉淀Mg2+,求出总的Mg2+,减去MgSO4中的Mg2+得到MgCl2的量
先用足量BaCl2溶液沉淀硫酸根离子,求出硫酸根离子的总量,并求出MgSO4的量,然后用足量NaOH溶液沉淀Mg2+,求出总的Mg2+,减去MgSO4中的Mg2+得到MgCl2的量
.

 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O