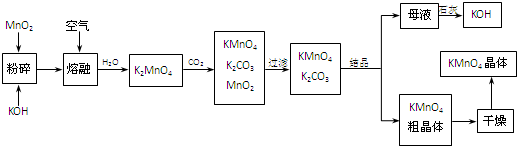
必考题高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.
(1)KMnO
4稀溶液是一种常用的消毒剂.其消毒机理与下列 (填序号)物质相似.
A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO
2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式: .
(3)向K
2MnO
4溶液中通入CO
2以制备KMnO
4,该反应中的还原剂是: .
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、 和 (写化学式).
(5)若不考虑物质循环与制备过程中的损失,则1mol MnO
2可制得 mol KMnO
4.





