
题目列表(包括答案和解析)
| ||
| ||
| ||
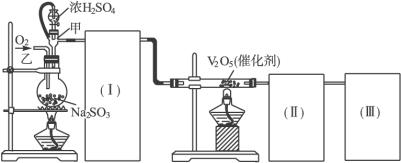
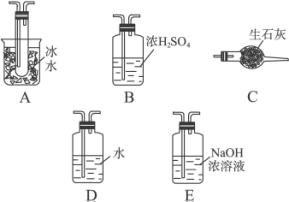
(1)根据实验的需要,(Ⅰ)(Ⅱ)(Ⅲ)处应连接合适的装置。请从下面装置中选择合适的装置,将其序号填入以下空格内:(Ⅰ) ;(Ⅱ) ;(Ⅲ) 。
(2)实验时,浓硫酸能顺利地滴入烧瓶中,甲仪器所起作用的原理是 。
(3)用大火加热烧瓶时,SO2的转化率会 (填“提高”“不变”或“降低”)。
(4)用a mol Na2SO3粉末与足量的浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ装置增重b g,则本实验中SO2的转化率为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com