
题目列表(包括答案和解析)
溶液配制及滴定:
(1)配制一定物质的量浓度的稀硫酸。
用24.5%硫酸(密度为![]() )配制100 mL 0.200
)配制100 mL 0.200![]() 硫酸时,需用酸式滴定管量取24.5%硫酸_______ mL,洗净的酸式滴定管应先 ,再用来量取所需的硫酸。
硫酸时,需用酸式滴定管量取24.5%硫酸_______ mL,洗净的酸式滴定管应先 ,再用来量取所需的硫酸。
(2)用已配好的0.200![]() 的硫酸溶液测定氢氧化钠样品中杂质氯化钠的含量。
的硫酸溶液测定氢氧化钠样品中杂质氯化钠的含量。
准确称取2.0克混有氯化钠的氢氧化钠固体试剂,将其配成100mL待测溶液,用浓度为0.200mol/L的标准硫酸酸溶液进行滴定,三次滴定的记录数据如下
| 实验编号 | 滴定开始时滴定管的读数为 | 滴定完成时,滴定管的读数为 | 待测溶液的体积 (mL) |
| 1 | 0.07 | 22.59 | 20.00 |
| 2 | 0.22 | 22.72 | 20.00 |
| 3 | 0.35 | 22.83 | 20.00 |
溶液配制及滴定:
(1)配制一定物质的量浓度的稀硫酸。
用24.5%硫酸(密度为)配制100mL 0.200
硫酸时,需用酸式滴定管量取24.5%硫酸_______ mL,洗净的酸式滴定管应先 ,再用来量取所需的硫酸。
(2)用已配好的0.200的硫酸溶液测定氢氧化钠样品中杂质氯化钠的含量。
准确称取2.0克混有氯化钠的氢氧化钠固体试剂,将其配成100mL待测溶液,用浓度为0.200mol/L的标准硫酸酸溶液进行滴定,三次滴定的记录数据如下
| 实验编号 | 滴定开始时滴定管的读数为
| 滴定完成时,滴定管的读数为 | 待测溶液的体积 (mL) |
| 1 | 0.07 | 22.59 | 20.00 |
| 2 | 0.22 | 22.72 | 20.00 |
| 3 | 0.35 | 22.83 | 20.00 |
测定出的氢氧化钠质量分数为 。
溶液配制及滴定:
(1)配制一定物质的量浓度的稀硫酸。
用24.5%硫酸(密度为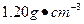 )配制100 mL 0.200
)配制100 mL 0.200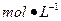 硫酸时,需用酸式滴定管量取24.5%硫酸_______ mL,洗净的酸式滴定管应先 ,再用来量取所需的硫酸。
硫酸时,需用酸式滴定管量取24.5%硫酸_______ mL,洗净的酸式滴定管应先 ,再用来量取所需的硫酸。
(2)用已配好的0.200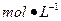 的硫酸溶液测定氢氧化钠样品中杂质氯化钠的含量。
的硫酸溶液测定氢氧化钠样品中杂质氯化钠的含量。
准确称取2.0克混有氯化钠的氢氧化钠固体试剂,将其配成100mL待测溶液,用浓度为0.200mol/L的标准硫酸酸溶液进行滴定,三次滴定的记录数据如下
| 实验编号 | 滴定开始时滴定管的读数为 | 滴定完成时,滴定管的读数为 | 待测溶液的体积 (mL) |
| 1 | 0.07 | 22.59 | 20.00 |
| 2 | 0.22 | 22.72 | 20.00 |
| 3 | 0.35 | 22.83 | 20.00 |
溶液配制及滴定:
(1)配制一定物质的量浓度的稀硫酸。
用24.5%硫酸(密度为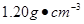 )配制100
mL 0.200
)配制100
mL 0.200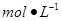 硫酸时,需用酸式滴定管量取24.5%硫酸_______ mL,洗净的酸式滴定管应先
,再用来量取所需的硫酸。
硫酸时,需用酸式滴定管量取24.5%硫酸_______ mL,洗净的酸式滴定管应先
,再用来量取所需的硫酸。
(2)用已配好的0.200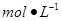 的硫酸溶液测定氢氧化钠样品中杂质氯化钠的含量。
的硫酸溶液测定氢氧化钠样品中杂质氯化钠的含量。
准确称取2.0克混有氯化钠的氢氧化钠固体试剂,将其配成100mL待测溶液,用浓度为0.200mol/L的标准硫酸酸溶液进行滴定,三次滴定的记录数据如下
|
实验编号 |
滴定开始时滴定管的读数为
|
滴定完成时,滴定管的读数为 |
待测溶液的体积 (mL) |
|
1 |
0.07 |
22.59 |
20.00 |
|
2 |
0.22 |
22.72 |
20.00 |
|
3 |
0.35 |
22.83 |
20.00 |
测定出的氢氧化钠质量分数为 。
实验室制备乙酸乙酯的反应和实验装置如下:
CH3COOH + C2H5OH  CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
投料 1 : 1 产率 65%
1 : 10 97%
(在120 ℃下测定)
已知:相关物理性质(常温常压)
| | 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | ~117 | 溶 |
| 乙酸乙酯 | 0.902 | ?84 | ~76.5 | 不溶 |




湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com