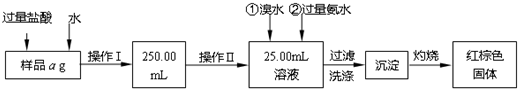
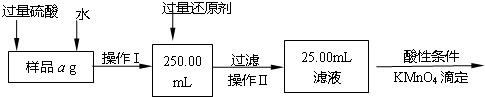
加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解.在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应.
(1)工业生产碘酸钾的流程如下:
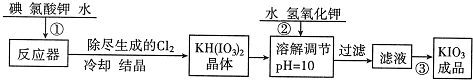
已知步骤①反应器中发生的反应为6I
2+11KClO
3+3H
2O=6KH(IO
3)
2+5KCl+3Cl
2↑.其中KH(IO
3)
2中I元素的化合价是
+5
+5
.碘酸钾的溶解度见表:
| 温度/℃ |
20 |
40 |
60 |
80 |
| KIO3/100gH2O |
8.08 |
12.6 |
18.3 |
24.8 |
操作③得到碘酸钾晶体的方法是
降温结晶
降温结晶
.
(2)加碘食盐中碘元素的测定.
①已知:KIO
3+5KI+3H
2SO
4=3K
2SO
4+3I
2+3H
2O;I
2+2S
2O
32-=2I
-+S
4O
62-学生甲设计的实验步骤如下:
步骤1:准确称取w g食盐,加适量蒸馏水使其完全溶解;
步骤2:用稀硫酸酸化所得食盐溶液,加入过量KI溶液充分混合;
步骤3:以淀粉为指示剂,逐滴加入2.0×10
-3 mol?L
-1的Na
2S
2O
310.0mL,恰好反应完全.则食盐样品中的碘元素含量是
mg?kg
-1(以含w的代数式表示).
②学生乙另取纯净的NaCl进行了下列实验:
| 实验步骤 |
实验操作 |
实验现象 |
| 步骤1 |
取1g纯净的NaCl,加3mL水配成溶液. |
溶液无变化 |
| 步骤2 |
滴入5滴淀粉溶液和1mL0.1 mol?L-1KI溶液,振荡. |
溶液无变化 |
| 步骤3 |
然后再滴入1滴1 mol?L-1的H2SO4,振荡. |
溶液变蓝色 |
实验中产生蓝色现象的可能原因是
4I-+4H++O2=2I2+2H2O
4I-+4H++O2=2I2+2H2O
(用离子方程式表示).
③根据学生乙的实验结果,学生甲测得的食盐中碘元素的含量可能
偏高
偏高
(填“偏高”、“偏低”或“准确”).原因是
过量的I-会被空气中的氧气氧化为I2
过量的I-会被空气中的氧气氧化为I2
.