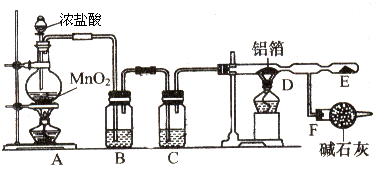
Ⅰ、(1)pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10
-3mol/L,则溶液中该溶质的pC=-lg10
-3=3.已知M
2CO
3为难溶物,则其K
SP的表达式为
Ksp=c2(M+)?c(CO32-)
Ksp=c2(M+)?c(CO32-)
_;现欲将某溶液中的M
+以碳酸盐(K
SP=1×10
-12)的形式沉淀完全,则最后溶液中的CO
32-的pC最大值为
2
2
(溶液中的离子浓度小于1×10
-5mol/L时,沉定完全).
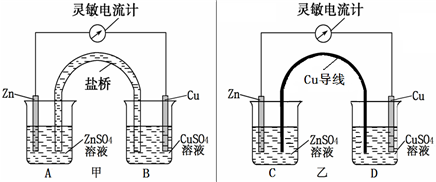
Ⅱ、某化学活动小组利用如下甲装置对原电池进行研究,请回答下列问题:(其中盐桥为含有饱和KCl溶液的琼脂)
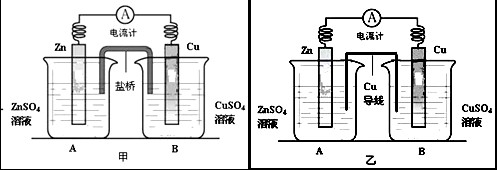
(2)在甲图装置中,当电流计中指针发生偏转时,盐桥中的K
+离子移向
B
B
烧杯(填“A”或“B”),装置中电子的移动路径和方向为_
由Zn电极沿导线流向Cu电极
由Zn电极沿导线流向Cu电极
该小组同学提出设想:如果将实验中的盐桥换为导线(铜制),电流表是否也发生偏转呢?带着疑问,该小组利用图乙装置进行了实验,发现电流计指针同样发生偏转.回答下列问题:
(3)对于实验中产生电流的原因,起初认为该装置仍然为原电池,但老师提醒注意使用的是铜导线,经深入探讨后认为烧杯A实际为原电池,对此问题上,该小组成员发生了很大分歧:
①一部分同学认为是由于ZnSO
4溶液水解显酸性,此时原电池实际是由Zn、Cu做电极,H
2SO
4溶液作为电解质溶液而构成的原电池.如果这个观点正确,写出烧杯B中铜片上发生反应的电极反应式为_
Cu2++2e-=Cu
Cu2++2e-=Cu
.
②另一部分同学认为是溶液酸性较弱,由于溶解在溶液中的氧气的作用,使得Zn、Cu之间形成原电池.如果这个观点正确,那么原电池的电极反应式为:正极:
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.
(4)若第(3)问中观点②正确,则可以利用此原理设计电池为在偏远海岛工作的灯塔供电.其具体装置为以金属铝和石墨为电极,以海水为电解质溶液,请写出该电池工作时总反应的化学方程式
4Al+3O2+6H2O=4Al(OH)3
4Al+3O2+6H2O=4Al(OH)3
.