
题目列表(包括答案和解析)
短周期元素A、B、C、D的原子序数依次增大,A、B同主族,A核外电子数等于其电子层数,C为元素周期表中原子半径最小的金属元素,D最外层电子数是其电子层数的3倍。填写下列空白。
(1)微粒半径比较:A- B+(填“>”、“<”或“=”)。
(2)A与D能组成化合物A2D和A2D2。A2D2的电子式为 。
A2D的沸点比D同主族其它元素与A组成的化合物的沸点高,原因是
。
(3)已知:在元素周期表中,有些元素的化学性质与其相邻左上方或右下方的另一主族元素的化学性质相似。则C构成的单质 (填“能”或“不能”)与强碱反应,B构成的单质在空气中充分燃烧,一定有或可能有的产物是 。
短周期元素A、B、C、D的原子序数依次增大,A、B同主族,A核外电子数等于其电子层数,C为元素周期表中原子半径最小的金属元素,D最外层电子数是其电子层数的3倍.填写下列空白.
(1)微粒半径比较:A-________B+(填“>”“=”或“<”).
(2)A与D能组成化合物A2D和A2D2.A2D的沸点比D同主族其他元素与A组成的化合物的沸点高,原因是________;A2D2的电子式为________.
(3)已知:ⅰ.3Mg+N2![]() Mg3N2;
Mg3N2;
ⅱ.在元素周期表中,有些元素的化学性质与其相邻左上方或右下方的另一主族元素的化学性质相似.
①C构成的单质________(填“能”或“不能”)与强碱溶液反应.
②B构成的单质在空气中充分燃烧的产物可能是________.
四种短周期元素A、B、C、D的原子序数依次递增.其中A、B、C三种元素基态原子的2p能级上都有未成对电子.且未成对电子个数分别是2、3、2;D与C 可以形成D2C和D2C2两种化合物。回答下列问题:
(1)已知A元素与氢元素形成的某种气态化合物在标准状况下的密度为1.161g/L,则在该化合物的分子中A原子的杂化方式为???? 。
(2)A、B、C二种元素的第一电离能由小到大的顺序为?????? (填元素符号)。
(3)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有I3、I4、I5……,推测D元素的电离能第一次突增应出现在第___电离能。
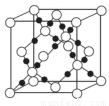
(4)AC2在高温高压下所形成的晶体其晶胞如图所示。该晶体的类型属于______________晶体.该晶体中A原子轨道的杂化类型为??????? 。
(5)C和C形成原子个数比为1:3的常见离子.推测这两种微粒的空间构型为???????????? 。
(6)C和D形成的一种离子化合物D2C的晶胞结构如图所示.该晶体中阳离子的配位数为?????? 。距一个阴离子周围最近的所有阳离子为顶点构成的几何体为????????? 。
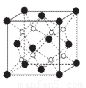
已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数为NA.则晶胞边长a=?? cm(用含ρ、NA的代数式表示)。
短周期元素A、B、C、D,原子半径依次增大,A、B在同一周期,B、C在同一主族,C元素原子核外电子数等于A、B元素原子核外电子数之和;C元素原子最外层电子数是D元素原子最外层电子数的4倍。请简答:
(1)B、C两元素的元素符号是:B__________,C_____ ___。
(2)B、C两元素的最高价氧化物的水化物的酸性由强到弱的顺序是________________。
(3)元素A和D按原子个数比为1 :1 ,形成的化合物的电子式为_______________;该物质为_________(填化合物类型),其化学键既有_________键,又有_______ 键。又知该化合物能跟A、B组成的某种化合物反应,生成A的单质,写出该反应的化学方程式:_____________________________________。
(4)A、B、D组成的一种常见化合物与A、C组成的常见化合物在一定条件下反应的化学方程式是:__________________________________________________。


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com