
题目列表(包括答案和解析)
为检验在空气中暴置过的过氧化钠的变质程度,某学习小组的甲、乙、丙三位同学经研究讨论,为减小实验的误差,分工协作如下:分别用等量的过氧化钠样品进行实验。
⑴甲同学采用如图实验装置,
甲同学测量气体时,实验过程中,量气管甲的前后示数差为473 mL(已折成标准状况下的体积), 实验后量气管甲中气体的主要成分有 。
⑵乙同学采用如图实验装置,
乙同学测量气体时,实验过程中,量气管甲的前后示数差为249 mL(已折成标准状况下的体积),乙同学的实验中,所用NaOH溶液的作用是:
① ;
② 。
⑶丙同学用浓度为1.00mol/L的标准盐酸滴定过氧化钠样品,应选用的玻璃仪器有:
。
从实验目的分析丙同学所采用的指示剂为 。丙同学实验完毕,从滴定管前后的示数得知消耗标准盐酸100.00 mL。
⑷利用上述实验数据,计算该过氧化钠样品变质的百分率为 。指导教师在批阅该实验小组的实验报告时,指出两点不足,可能引起实验误差:
① ;
② 。
为检验在空气中暴置过的过氧化钠的变质程度,某学习小组的甲、乙、丙三位同学经研究讨论,为减小实验的误差,分工协作如下:分别用等量的过氧化钠样品进行实验。
⑴甲同学采用如图实验装置,
甲同学测量气体时,实验过程中,量气管甲的前后示数差为473 mL(已折成标准状况下的体积),实验后量气管甲中气体的主要成分有 。
⑵乙同学采用如图实验装置,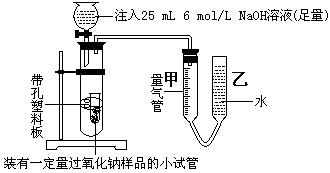
乙同学测量气体时,实验过程中,量气管甲的前后示数差为249 mL(已折成标准状况下的体积),乙同学的实验中,所用NaOH溶液的作用是:
① ;
② 。
⑶丙同学用浓度为1.00 mol/L的标准盐酸滴定过氧化钠样品,应选用的玻璃仪器有:
。
从实验目的分析丙同学所采用的指示剂为 。丙同学实验完毕,从滴定管前后的示数得知消耗标准盐酸100.00 mL。
⑷利用上述实验数据,计算该过氧化钠样品变质的百分率为 。指导教师在批阅该实验小组的实验报告时,指出两点不足,可能引起实验误差:
① ;
② 。
为检验在空气中暴置过的过氧化钠的变质程度,某学习小组的甲、乙、丙三位同学经研究讨论,为减小实验的误差,分工协作如下:分别用等量的过氧化钠样品进行实验。
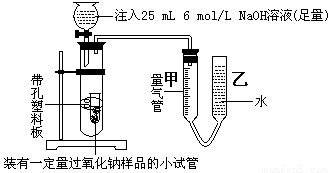
⑴甲同学采用如图实验装置,
甲同学测量气体时,实验过程中,量气管甲的前后示数差为473 mL(已折成标准状况下的体积), 实验后量气管甲中气体的主要成分有 。
⑵乙同学采用如图实验装置,
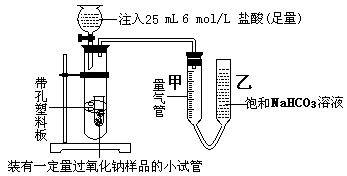
乙同学测量气体时,实验过程中,量气管甲的前后示数差为249 mL(已折成标准状况下的体积),乙同学的实验中,所用NaOH溶液的作用是:
① ;
② 。
⑶丙同学用浓度为1.00 mol/L的标准盐酸滴定过氧化钠样品,应选用的玻璃仪器有:
。
从实验目的分析丙同学所采用的指示剂为 。丙同学实验完毕,从滴定管前后的示数得知消耗标准盐酸100.00 mL。
⑷利用上述实验数据,计算该过氧化钠样品变质的百分率为 。指导教师在批阅该实验小组的实验报告时,指出两点不足,可能引起实验误差:
① ;
② 。
为检验在空气中暴置过的过氧化钠的变质程度,某学习小组的甲、乙、丙三位同学经研究讨论,为减小实验的误差,分工协作如下:分别用等量的过氧化钠样品进行实验。
⑴甲同学采用如图实验装置,
甲同学测量气体时,实验过程中,量气管甲的前后示数差为473 mL(已折成标准状况下的体积), 实验后量气管甲中气体的主要成分有 。
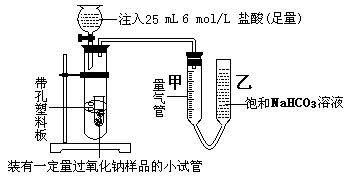
⑵乙同学采用如图实验装置,
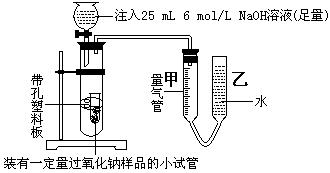
乙同学测量气体时,实验过程中,量气管甲的前后示数差为249 mL(已折成标准状况下的体积),乙同学的实验中,所用NaOH溶液的作用是:
① ;
② 。
⑶丙同学用浓度为1.00 mol/L的标准盐酸滴定过氧化钠样品,应选用的玻璃仪器有:
。
从实验目的分析丙同学所采用的指示剂为 。丙同学实验完毕,从滴定管前后的示数得知消耗标准盐酸100.00 mL。
⑷利用上述实验数据,计算该过氧化钠样品变质的百分率为 。指导教师在批阅该实验小组的实验报告时,指出两点不足,可能引起实验误差:
① ;
② 。
 某课外活动小组准备用如图所示的装置进行实验.现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:
某课外活动小组准备用如图所示的装置进行实验.现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:| A电极 | B电极 | X溶液 | |
| 甲 | Cu | Zn | H2SO4 |
| 乙 | Pt | Pt | CuCl2 |
| 丙 | Fe | Cu | ? |
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com