
题目列表(包括答案和解析)
| |||||||||||||||||||||||
一、实验用品:纯锌片,铜片,37%的浓盐酸,蒸馏水,氯化铜溶液。
二、实验记录:
交流卡片 NO:2006—SY—518 主题:Zn,Cu与浓盐酸 A.将锌放入浓盐酸中,反应较快 B.将锌片与铜片贴在一起,一同投入浓盐酸中,反应快速放出气体 C.当B中锌片完全溶解后,将溶液加热,又产生气体(值得进一步探究),得到无色溶液 D.将上述反应后的溶液,隔绝空气,加入适量水,出现白色沉淀 |
三、提供资料:
资料卡片 NO:2006—ZL—918 主题:生成一价铜的反应 ①课本上:CH3CHO+2Cu(OH)2 ②盐城市第二次调研试卷:Cu2++4I-====2CuI(白色)↓+I2 ③《无机化学》下册,p788,氯化亚铜在不同浓度的KCl溶液中可形成[CuCl2]-、[CuCl3]2-、[CuCl4]3-等离子,且它们在溶液中均为无色。 |
四、请你参与以下探究:
(1)交流卡片中,实验A反应速率明显比B小,原因是:___________________________。
(2)根据铜位于金属活动顺序表氢之后,与稀盐酸不反应,依据交流卡片C又产生气体的事实。作出如下推断:
①有同学认为是溶解在溶液中的H2逸出,你认为是否有道理,理由是:__________________。
②某同学作了如下猜想,是否成立,请你设计实验方案加以验证:
猜想 | 验证方法 | 预测现象及结论 |
认为铜片中可能含有锌等杂质 |
|
|
(3)交流卡片D中的白色沉淀,分析:不可能是CuCl2,因为CuCl2溶液显蓝色或绿色,也不可能是氯化锌,因为稀释后溶液更稀,不会产生出沉淀。并利用资料①②大胆猜想,白色沉淀是生成的氯化亚铜。请你帮他设计验证方案(若有多个,只设计两个方案):
| 预设验证方法 | 预测的现象与结论 |
白色沉淀是氯化亚铜 |
|
|
|
|
(4)指导老师肯定了白色沉淀是氯化亚铜,请结合资料卡片③,写出铜与足量盐酸在加热条件下反应生成无色溶液及气体的化学方程式:___________________。根据交流卡片D,生成沉淀,实际上是一个平衡问题,请写出这一平衡关系式:___________________(用离子方程式表示)。
(5)就铜与浓盐酸反应若还需进一步探讨,你认为还可探究的内容有:___________________(只提供一个实验课题即可)。
随着铅蓄电池的广泛应用,使回收利用铅资源成为重要课题。某研究性学习小组利用废旧铅蓄电池阴、阳极填充物(铅膏)制备塑料加工热稳定剂三盐基硫酸铅,实验流程如下:
(1)物质X是一种可循环利用的物质,该物质是 。
(2)生成三盐基硫酸铅的反应的离子方程式为 。
(3)将滤液I和滤液Ⅱ合并后可用来提取一种钠盐副产品(相对分子质量为322),已知副产品带10个结晶水的结晶水合物,则其化学式 ,由滤液提取该副产品的主要实验步骤依次为 、 、过滤、洗涤、干燥。
(4)过滤时洗涤沉淀(或固体)的操作方法是 。
(5)向铅膏浆液中加入Na2SO3溶液的目的是将PbO2还原为PbO,若实验中所取铅膏浆液质量为47.8g,其中PbO2的质量分数为15.0%,要将PbO2还原,至少需要加入
mL1.0mol·L-1Na2SO3溶液。
随着铅蓄电池的广泛应用,使回收利用铅资源成为重要课题。某研究性学习小组利用废旧铅蓄电池阴、阳极填充物(铅膏)制备塑料加工热稳定剂三盐基硫酸铅,实验流程如下: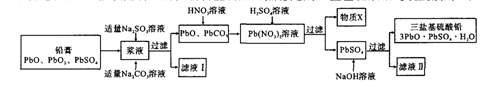
(1)物质X是一种可循环利用的物质,该物质是 。
(2)生成三盐基硫酸铅的反应的离子方程式为 。
(3)将滤液I和滤液Ⅱ合并后可用来提取一种钠盐副产品(相对分子质量为322),已知副产品带10个结晶水的结晶水合物,则其化学式 ,由滤液提取该副产品的主要实验步骤依次为 、 、过滤、洗涤、干燥。
(4)过滤时洗涤沉淀(或固体)的操作方法是 。
。
(5)向铅膏浆液中加入Na2SO3溶液的目的是将PbO2还原为PbO,若实验中所取铅膏浆液质量为47.8g,其中PbO2的质量分数为15.0%,要将PbO2还原,至少需要加入
mL1.0mol·L-1Na2SO3溶液。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com