
题目列表(包括答案和解析)
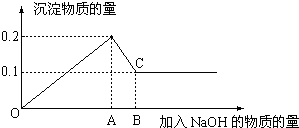
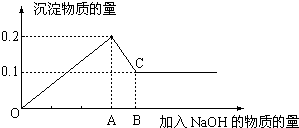 在MgCl2和AlCl3的混和溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如图所示,则:
在MgCl2和AlCl3的混和溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如图所示,则: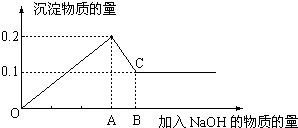
 (1)现将8.4g CO2和H2O的混合气体,通入足量的Na2O2中,可得O2(标准状况)2.8L,求原混合气体中CO2与H2O的物质的量各是多少?
(1)现将8.4g CO2和H2O的混合气体,通入足量的Na2O2中,可得O2(标准状况)2.8L,求原混合气体中CO2与H2O的物质的量各是多少?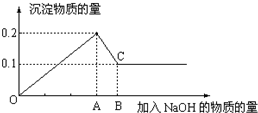 Ⅰ用元素符号或化学式回答原子序数11~18的元素的有关问题:
Ⅰ用元素符号或化学式回答原子序数11~18的元素的有关问题:在铁和铜的混和物中,加入一定量的稀硝酸,使之充分反应,剩余金属m1 g,再向其中加入一定量的稀硫酸,充分振荡后,剩余金属m2 g,则m1与m2关系是
A.m1一定大于m2 B.m1可能大于m2
C.m1可能等于m2 D.m1一定等于m2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com