[化学--选修物质结构与性质]
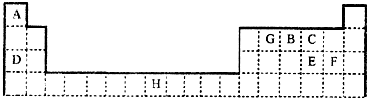
已知A、B、C、D、E、F、G位于元素周期表的前四周期,且元素原子序数依次增加,A焰色反应呈黄色;工业常用电解B的熔融的氯化物来制备B,C是一种能被HF和NaOH溶液溶解的单质,D的电负性比磷大,第一电离能却比磷小,E单质是制备漂白液的原料,F能形成红色(或砖红色)和黑色的两种氧化物,G是一种主族金属.
(1)前四周期所有元素中,基态原子中未成对电子与其所在周期数相同的元素有
种.
(2)元素A、B、C分别与氟气化合形成物质X、Y、Z熔点见下表:
| 氟化物 |
X |
Y |
Z |
| 熔点/K |
1266 |
1534 |
183 |
解释表中氟化物熔点差异的原因:
.
(3)已知常温条件下,极性分子DOE
2是一种液态化合物,中心原子D的杂化方式是
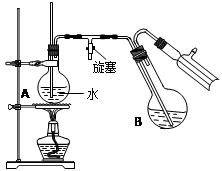
.向盛有10mL水的锥形瓶中滴加少量的DOE
2溶液,生成两种有刺激性气味的气体.请书写此反应的化学方程式
.
(4)G与氮原子可1:1化合,形成人工合成的新型半导体材料,其晶体结构与单晶硅相似.G原子的价电子排布式为
.在该合成材料中,与同一个G原子相连的N原子构成的空间构型为正四面体.在四种基本晶体类型中,此晶体属于
晶体.
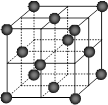
(5)F晶体的堆积方式是
(填堆积名称),其配位数为
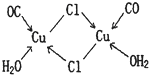
. 向F的硫酸盐溶液中滴加氨水直至过量,写出此过程所涉及的两个离子方程式
根据价层电子对互斥理论,预测SO
42-的空间构型为
.