
题目列表(包括答案和解析)
| 实验操作 | 实验现象 |
| 1.用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移 动,随之消失,溶液变红色 (B)产生气体,可在空气中燃烧,溶液变成浅红色 (C)反应不十分强烈,产生的气体可以在空气中燃 烧 (D)剧烈反应,产生可燃性气体 (E)溶液的碱性逐渐减弱 (F)生成淡黄色沉淀 |
| 2.向新制的H2S饱和溶液中滴加新制的氯水 | |
| 3.钠与滴有酚酞试液的冷水反应 | |
| 4.镁带与2mol.L-1的盐酸反应 | |
| 5.铝条与2mol.L-1的盐酸反应 | |
| 6.测定 0.1mol/L的Na2SiO3、Na3PO4、Na2SO4溶液的pH |
| 实验操作 | 实验现象 |
| 1.用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移 动,随之消失,溶液变红色 (B)产生气体,可在空气中燃烧,溶液变成浅红色 (C)反应不十分强烈,产生的气体可以在空气中燃 烧 (D)剧烈反应,产生可燃性气体 (E)溶液的碱性逐渐减弱 (F)生成淡黄色沉淀 |
| 2.向新制的H2S饱和溶液中滴加新制的氯水 | |
| 3.钠与滴有酚酞试液的冷水反应 | |
| 4.镁带与2mol.L-1的盐酸反应 | |
| 5.铝条与2mol.L-1的盐酸反应 | |
| 6.测定 0.1mol/L的Na2SiO3、Na3PO4、Na2SO4溶液的pH |
| 实验操作 | 实验现象 |
| 1.用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移 动,随之消失,溶液变红色 (B)产生气体,可在空气中燃烧,溶液变成浅红色 (C)反应不十分强烈,产生的气体可以在空气中燃 烧 (D)剧烈反应,产生可燃性气体 (E)溶液的碱性逐渐减弱 (F)生成淡黄色沉淀 |
| 2.向新制的H2S饱和溶液中滴加新制的氯水 | |
| 3.钠与滴有酚酞试液的冷水反应 | |
| 4.镁带与2mol.L-1的盐酸反应 | |
| 5.铝条与2mol.L-1的盐酸反应 | |
| 6.测定 0.1mol/L的Na2SiO3、Na3PO4、Na2SO4溶液的pH |
| 实验操作 | 实验现象 |
| 1.用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移 动,随之消失,溶液变红色 (B)产生气体,可在空气中燃烧,溶液变成浅红色 (C)反应不十分强烈,产生的气体可以在空气中燃 烧 (D)剧烈反应,产生可燃性气体 (E)溶液的碱性逐渐减弱 (F)生成淡黄色沉淀 |
| 2.向新制的H2S饱和溶液中滴加新制的氯水 | |
| 3.钠与滴有酚酞试液的冷水反应 | |
| 4.镁带与2mol.L-1的盐酸反应 | |
| 5.铝条与2mol.L-1的盐酸反应 | |
| 6.测定 0.1mol/L的Na2SiO3、Na3PO4、Na2SO4溶液的pH |
有趣的化学实验能激发学生学习化学的兴趣,提高学习积极性,同时也活跃课堂气氛。在中学化学教材中,可以挖掘许多有趣的实验,例如:
Ⅰ.[火球游泳]水火不相容,这是人们公认的常识,从来没有看见过火球能在水面上游来游去。然而,某化学兴趣小组的同学,做了一个“火球游泳”小魔术。他在一个100毫升的烧杯里面装上自来水,然后用镊子将一块豆粒大的金属钾,轻轻地放在烧杯里,这时,烧杯里的水面上立刻生成个火球,这个火球在水面上滚来滚去,同时发生嗤嗤的响声,场景十分壮观。
Ⅱ.[“蓝瓶子”实验]在250 mL平底烧瓶中依次加入2 g氢氧化钠、100 mL蒸馏水、2 g葡萄糖(粉末),振荡使其溶解。滴入4~6滴0.2%的亚甲基蓝溶液,塞上瓶塞(如图),振荡烧瓶,溶液呈蓝色。静置,约3分钟后蓝色消失,变为无色。再次振荡,无色溶液又呈蓝色。可反复多次。已知:亚甲基蓝容易被还原。根据上述实验,回答下列问题:
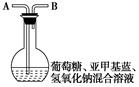
(1)实验室中金属钾应保存在______________________,原因是________________________________;化学兴趣小组的同学取出一小粒金属钾的操作是________________________________________________________________________
________________________________________________________________________。
(2)写出Ⅰ中金属钾发生反应的离子方程式: __________________________________
________________________________________________________________________。
(3)为探究“蓝瓶子”实验是什么原因引起的,某同学做了以下实验:
A.从烧瓶中取出溶液注满一支试管,塞上橡皮塞。试管中的溶液由蓝色变为无色,再振荡试管溶液不能变蓝。
B.在原烧瓶中经A处鼓入空气,溶液又慢慢变蓝了。静置片刻后,蓝色又消失。再次鼓入空气,又慢慢变蓝。
C.为了进一步弄清是何种成分引起的,他又继续探索。从A处改通纯净的N2、CO2,都不能使烧瓶中的无色溶液变蓝。把制得的氧气从A处通入,发现上述无色溶液慢慢变为蓝色。
到此为止,“蓝瓶子”实验原理有了科学结论,请你总结“蓝瓶子”实验的变色原理:________________________________________________________________________
________________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com