
题目列表(包括答案和解析)
 (2011?万州区一模)Ⅰ、铁单质及其化合物在生活生产中应用广泛.如硫酸铁可作絮凝剂,常用于净水,其原理是(用离子方程式表示)
(2011?万州区一模)Ⅰ、铁单质及其化合物在生活生产中应用广泛.如硫酸铁可作絮凝剂,常用于净水,其原理是(用离子方程式表示) Fe(OH)3+3H+
Fe(OH)3+3H+ Fe(OH)3+3H+
Fe(OH)3+3H+ (1)未用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑.则铁锅的锈蚀属于
(1)未用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑.则铁锅的锈蚀属于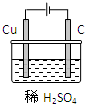

 (1)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
(1)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题: ( I)在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的交化如下表:
( I)在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的交化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
| c2(NO2) |
| c2(NO)?c(O2) |
| c2(NO2) |
| c2(NO)?c(O2) |
| ||
| ||
| ||
| ||
| 序号 | 铁丝状态 | 温度℃ | 气流湿度 | 气流成分 | 时间 | 现象 |
| ① | 洁净光亮 | 25 | 干燥 | 空气 | 一个月 | 铁丝表面光亮 |
| ② | 洁净光亮 | 25 | 潮湿 | 空气 | 一天 | 铁丝表面光亮 |
| ③ | 洁净光亮 | 25 | 潮湿 | 空气 | 一个月 | 铁丝表面已经变暗 |
| ④ | 洁净光亮 | 25 | 潮湿 | 氧气 | 一天 | 铁丝表面略微变暗 |
| ⑤ | 洁净光亮 | 40 | 潮湿 | 氧气 | 一天 | A |
| ⑥ | 光亮铁丝表面有氯化钠溶液 | 25 | 潮湿 | 氧气 | 一天 | 铁丝表面变暗程度比④严重 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com